Значение - свободная энергия - образование
Cтраница 1
Значения свободной энергии образования окислов приведены для 298 К, однако для некоторых окислов указаны значения свободной энергии и для более высоких температур. [1]
Значения свободной энергии образования сернистых соединений, приведенные в табл. 1, показывают, что меркаптаны, сульфиды и гетероциклические сернистые соединения при 1000 К являются неустойчивыми по отношению к распаду на элементы. При 298 16 К неустойчивыми к распаду на элементы являются сульфиды и в более сильной степени гетероциклические соединения. [2]
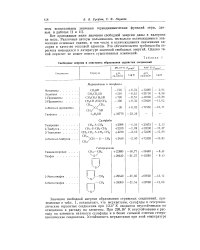 |
Свободные энергии и константы образования сернистых соединений. [3] |
Значения свободной энергии образования сернистых соединений, приведенные в табл. 1, показывают, что меркаптаны, сульфиды и гетероциклические сернистые соединения при 1ССО К являются неустойчивыми по отношению к распаду на элементы. При 298 16 К неустойчивыми к распаду на элементы являются сульфиды и в более сильной степени гетероциклические соединения. [4]
Ниже приведены значения свободной энергии образования наиболее важных углеводородов, с которыми приходится встречаться при крекинг-процессах. Уравнения, представленные в табл. 18 [1], даны в упрощенной форме, которая, однако, вполне достаточна для наших целей. Имеются сведения о свободной энергии образования газообразных углеводородов из графита и газообразного водорода при температурах 700 - 1000 К. [5]
Из полученных ранее значений свободной энергии образования карбида циркония и значений давления пара циркония при 2600 К равновесное парциальное давление Zrraa было найдено равным 8 - 10 - 9 атм. Таким образом, карбид циркония, насыщенный углеродом, теряет преимущественно углерод. Из этого следует, что карбид должен давать сублимат постоянного состава. [6]
Вследствие этого ниже приводятся значения свободной энергии образования наиболее важных углеводородов и некоторых неорганических веществ, с которыми приходится иметь дело при процессах крекинга. Помещенные в табл. 22 данные [1] показывают изменения свободной энергии образования газообразных углеводородов ( если нет оговорки) из графита и газообразного водорода в температурном интервале 700 - 1000 К. [7]
Вследствие этого ниже приводятся значения свободной энергии образования наиболее важных углеводородов и некоторых неорганических веществ, с которыми приходится иметь дело при процессах крекинга. Помещенные в табл. 22 данные [1] показывают изменения свободной энергии образования газообразных углеводородов ( если нет оговорки) из графита и газообразного водорода в температурном интервале 700 - 1000 К. [8]
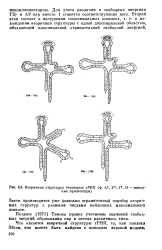 |
Вторичные структуры некоторых тРНК ( ф, А, У, Г, И - минорные нуклеотиды. [9] |
Позднее ( 1971) Тиноко провел уточнение значений свободных энергий образования пар и петель различного типа. [10]
Показано, что, несмотря на большую разницу значений свободной энергии образования указанных углеводородов и метана, степени превращения их в ацетилен отличаются незначительно. Невелика также и разница в температурах, необходимых для достижения одинаковой степени превращения различных углеводородов в ацетилен. Тем ле менее, с энергетической точки зрения термоокислительный пирэлиз этана, пропана и бутана является более выгодным, чем пиролиз метана. [11]
Интересно отметить, что, несмотря а большую разницу значений свободной энергии образования CHU, C Hg, СзН8 и С4Ню, степень превращения этих углеводородов в ацетилен отличается незначительно. Вследствие этого незначительна и разница температур, необходимых для достижения одинаковой степени превращения различных углеводородов в ацетилен. Так, если метан превращается в ацетилен на 95 % при температуре 1745 К, то для наиболее тяжелого углеводорода-бутана - соответствующая температура составляет 1680 К, то есть разница составляет всего лишь 65 К. [12]
Интересен в качестве примера сборник [20], в котором в ряде статей о значениях свободной энергии образования карбидов, нитридов и других соединений приведены уравнения типа ZrN Zr V2N2 или ZrC Zr С. [13]
Ремоло Циола [14], имея в виду, что при расчете по методу [12] и [13] необходимо вычислять отдельно значения свободной энергии образования всех соединений ( молекул) как вступающих в реакцию, так и получающихся в результате реакции, несколько видоизменил вышеуказанный. [14]
Далее, предположение, что свободная энергия образования гид-ратированного иона водорода в водном растворе также равна нулю, позволяет оценить значения свободной энергии образования всех других ионов в водных растворах. [15]
Страницы: 1 2