Значение - энтальпии
Cтраница 2
Значения энтальпии на входе и выходе в уравнении (VII.11) рассчитывают в модуле расчета энтальпии библиотеки ФИЗХИМ. Эту задачу полностью решает программа РАВНОХИМ. [16]
Значения энтальпии ( Л 421 кДж / кг и / 2462 кДж / кг) взяты из Приложения 25 по метану. [17]
 |
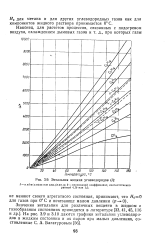
Кривые зависимости величин i, r и i от давления для водяного пара. [18] |
Значения энтальпии, энтропии и удельных объемов некипящей воды и перегретого пара находят по таблицам, которые в данном учебнике не приведены, но имеются в ряде учебников и пособий по технической термодинамике. [19]
Значения энтальпии на выходе из системы принимают со знаком плюс, а на входе - со знаком минус. Уравнение первого закона термодинамики в виде ( 5) широко используют при составлении энергетических балансов технических систем. [20]
Значения энтальпии ( J [ 421 кДж / кг и J2462 кДж / кг) взяты по метану. [21]
Значения энтальпии в начале и конце газопровода ( is, IK) определяются в зависимости от состава газа, давления и температуры. [22]
Значение энтальпии для CH3F приводит к величине энергии связи С-F, равной 443 кДж - моль-1. Это значение дано в табл. V.I. Другие фторзамещенные метана стабилизированы вследствие резонанса со структурами, отличающимися от структур с нормальными валентными связями. [23]
Значения энтальпии легко найти из термодинамических таблиц или диаграмм. Если отсутствуют обычные таблицы или графики термодинамических величин, то количество тепла можно вычислить из теплоемкости и скрытой теплоты, а работу - из уравнений, выведенных в гл. [24]
Значения энтальпии ( Л 421 кДж / кг и / 2462 кДж / кг) взяты из Приложения 25 по метану. [25]
 |
Расчет массового состава исходного газа. [26] |
Значения энтальпии ( Ii f 421 кДж / кг и 12462 кДж / кг) взяты по метану. [27]
Значения энтальпии и энтропии образования дефекта по Френкелю найдены равными 1 44 эВ и 4 1 10 - 4 эВ / град. [28]
Значения энтальпии в работах НИИВТ [27], а также Новикова и Груздева [49, 50] согласуются между собой и с данными НБС в пределах погрешности экспериментов. В своей последней работе Эвинг с сотрудниками [51], применив медный блок-калориметр, измерил энтальпию натрия до 1400 К. Данные [51] с погрешностью 1 5 % соответствуют экстраполированному уравнению НБС. Теплота плавления щелочных металлов L при 1300 и 1400 К была получена по этому уравнению: Li - 717; Na - 622; К - 559; Rb - 524; Cs - 499 ккал / кмоль. Вычисленные нами значения термодинамических функций натрия несколько отличаются от приведенных в [5] по той же причине, что и для лития. [29]
 |
Энтальпия жидких углеводородов ( г. [30] |
Страницы: 1 2 3 4