Результат - измерение - активность
Cтраница 2
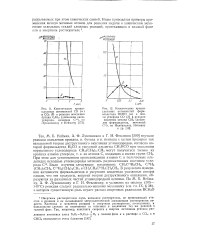
Наиболее простой вид кривые радиометрического титрования имеют, если, во-первых, растворимость образующегося при реакции соединения незначительна, так что неполнота осаждения не сказывается на результатах измерения активности раствора /, и, во-вторых, объем прибавляемого к анализируемой пробе реагента столь мал, что общий объем раствора в ходе титрования можно считать постоянным. При этих условиях кривая радиометрического титрования состоит из двух прямолинейных участков. В тех случаях, когда изменением объема пренебречь нельзя, в результаты измерения / следует вводить поправку на разбавление. [16]
В результате измерения активности формальдегида и уксусного альдегида указанные авторы нашли, что эти продукты, вопреки теории деструктивного окисления, образуются из различных частей углеводородной цепочки. Луковникову и Г. И. Феклисову, в условиях их опытов t Uo - 340 С) реакция следует радикально-цепному механизму ( см. гл. [18]
В данном случае в процессе измерения клетка находится в неизменном функциональном состоянии. Таким образам гарантируется высокая воспроизводимость1 результатов измерения активности биологически активных веществ, создается предпосылка для создания шкалы активности изучаемых1 веществ, например шкалы по глутамату натрия. Это позволяет внедрить точные количественные методы в; фармакологические исследования вновь синтезированных лекарственных средств. [19]
Вычисляют количество выделенного иттрия. Для получения выходов иттрия и стронция исправляют результат измерения активности иттрия на нулевое время. [20]
Пробы для анализа отбирали и из всего электролита, и из слоев, образующихся после отгонки метанола и разделения продуктов электролиза водой. Отбор проб строго фиксировали во времени, и результаты измерения активности пересчитывали к начальному времени ( / 0) электролиза. [21]
Для этого вносят в мерную колбу на 25 мл 0 1 мл исходного раствора, доводят объем жидкости в колбе до метки насыщенным при комнатной температуре раствором Ba ( NO3) 2 и перемешивают. На основании результатов измерения активности рассчитывают объем исходного раствора, который обеспечил бы активность - 4 - 103 имп / мин. [22]
Чэпмен и Хэйр [34] исследовали роль гидроксильных групп на поверхности катализатора из пористого стекла в каталитическом крекинге кумола. Основываясь на результатах измерения активности и других данных, авторы высказали предположение о том, что на поверхности катализатора присутствуют только кислотные центры бренстедовского типа; центры льюисов-ского типа не удалось обнаружить ни химическим анализом, ни методом ЭПР. [23]
Час ицы, образующиеся при распаде атомов радиоактивных элементов, испускаются по всем направлениям. Так как образец радиоактивного элемента нанесен на какое-либо вещество, то происходит рассеяние электронов материалом подкладки. Это рассеяние влияет на число электронов, идущих в направлении счетной трубки установки, и, следовательно, влияет на результаты измерения активности. [24]
 |
Электрод для независимого введения в плазму паров носителя и примесей. [25] |
Влияние носителя на скорость испарения некоторых примесей из пробы U3O8 в дуге постоянного тока было проверено также с помощью радиоактивных индикаторов. Опыт был поставлен гак же, как и описанный выше. После того как дуга горела в течение 30 сек. Результаты измерений активности проб, представленные в табл. 27, подтверждают вывод о том, что носитель не оказывает действия на ход испарения примесей. [26]
В этих условиях любое измерение растворимости, естественно, становится ошибочным. Поэтому при каждой операции с раствором проверяют, сохраняется ли насыщение. На основании результатов измерения активности образца сравнения и насыщенных растворов вычисляют растворимость в миллиграммах на 100 мл и миллимолях на литр. [27]
Определение коэффициента самодиффузии твердых веществ методом снятия слоев. Образец в инертной атмосфере нагревают до температуры Т, при которой хотят определить коэффициент самодиффузии, и выдерживают его при этой температуре в течение времени t, достаточного для проникновения радиоактивных атомов на заметное расстояние от поверхности образца. Так как диффузия на поверхности протекает с иной скоростью, чем в объеме, остывший до комнатной температуры образец обтачивают с краев и затем определяют концентрацию радиоактивных атомов на различной глубине образца. С этой целью на токарном станке, микротомом, электрохимически, растворением в кислоте или каким-либо иным путем снимают тонкие слои ( толщиной от нескольких микрон до - 100 микрон) вещества и определяют их активность. Зная точную толщину каждого слоя, по результатам измерения активности находят зависимость концентрации диффундировавшего изотопа от расстояния. [28]
Подготовка к анализу радио-хроматографическим методом и методика самого анализа заключаются в следующем. Если в качестве осадителя был взят гидрофосфат натрия Na2HPO4) то в колонке образуется зона фосфата кобальта. Для исследования распределения осадка вдоль зоны ( степени равномерности распределения) стеклянную колонку разрезают и из цилиндрической ее части выталкивают стеклянным пестиком столбик сорбента на стеклянную пластинку. Затем разрезают этот столбик на равные части, так чтобы получились диски толщиной, например, по 2 мм каждый. Отдельные диски ( таблетки) переносят на алюминиевые пластинки, высушивают, взвешивают ( обычно на торзионных весах), измельчают и распределяют равномерным слоем на определенной поверхности ( 1 - 2 еж2), после чего измеряют радиоактивность с помощью счетчика Гейгера-Мюллера. В заключение по результатам измерения активности различных, последовательно расположенных слоев по длине зоны в колонке строят кривую распределения осадка Со3 ( Р04) 2 в координатах миллиграмм-эквивалент вещества на 1 г носителя - масса зоны, г ( или длина зоны, мм), при условии, что начало оси координат соответствует верхней части колонки. [29]
Подготовка к анапизу радио-хроматографическим методом и методика самого анализа заключаются в следующем. Если в качестве осадителя был взят гидрофосфат натрия Na2HPO4, то в колонке образуется зона фосфата кобальта. Для исследования распределения осадка вдоль зоны ( степени равномерности распределения) стеклянную колонку разрезают и из цилиндрической ее части выталкивают стеклянным пестиком столбик сорбента на стеклянную пластинку. Затем разрезают этот столбик на равные части, так чтобы получились диски толщиной, например, по 2 мм каждый. Отдельные диски ( таблетки) переносят на алюминиевые пластинки, высушивают, взвешивают ( обычно на торзионных весах), измельчают и распределяют равномерным слоем на определенной поверхности ( 1 - 2 еж2), после-чего измеряют радиоактивность с помощью счетчика Гейгера-Мюллера. В заключение по результатам измерения активности различных, последовательно расположенных слоев по длине зоны в колонке строят кривую распределения осадка Со3 ( РО4) 2 в координатах миллиграмм-эквивалент вещества на 1 г носителя - масса зоны, г ( или длина зоны, мм), при условии, что начало оси координат соответствует верхней части колонки. [30]
Страницы: 1 2