Результат - спектрофотометрическое измерение
Cтраница 1
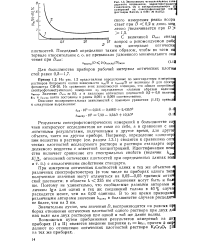 |
Зависимость относительного стан дартного отклонения, характеризующег сходимость ( / и воспроизводимость ( J измерений на спектрофотометре СФ-Й ( растворы КгСпО. в 0 005 Л1 HjSO. [1] |
Результаты спектрофотометрических измерений в большинстве ел; чаев интересуют исследователя не сами по себе, а в сравнении с ан; логичными результатами, полученными в другое время, для другог объекта, часто на другом приборе. Например, определение концентр, ции вещества в растворе ( см. раздел 1.3.1) сводится к сравнению опт ] ческих плотностей исследуемого раствора и раствора стандарта onpi деляемого вещества с известной концентрацией. [2]
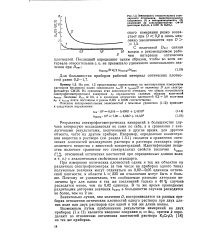 |
Зависимость относительного стандартного отклонения, характеризующего сходимость ( / и воспроизводимость ( 2 измерений на спектрофотометре СФ-2 & ( растворы КгСГгО, в 0 005 М HiSO. [3] |
Результаты спектрофотометрических измерений в большинстве случаев интересуют исследователя не сами по себе, а в сравнении с аналогичными результатами, полученными в другое время, для другого объекта, часто на другом приборе. Например, определение концентрации вещества в растворе ( см. раздел 1.3.1) сводится к сравнению оптических плотностей исследуемого раствора и раствора стандарта определяемого вещества с известной концентрацией. [4]
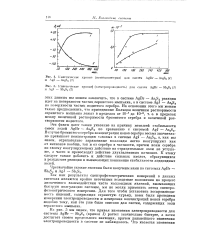 |
Кинетические кривые ( потонциометрия для систем AgBr - As2S3 ( 1. и AgJ - As2S3 ( 2.| Кинетические кривые ( электропроводность для систем AgBr - Sb2S3 ( 1. и AgJ - Sb2S3 ( 2. [5] |
Так как результаты спектрофотометрических измерений в данных системах являются крайне неточными вследствие наложения на процесс химического взаимодействия чисто коллоидных явлений, вызывающих быструю коагуляцию системы, мы не могли применить метод спектро-фотометрического измерения. Для того чтобы установить воспроизводимость явлений, содержащих сернистую сурьму, нами были проведены измерения электропроводности и измерения концентраций ионов серебра подобно тому, как это уже было описано для систем, содержащих золи сернистого мышьяка. [6]
Перечислим основные факторы, влияющие на воспроизводимость результатов спектрофотометрического измерения. [7]
 |
Блок-схема двухлучевого спектрофотометра. [8] |
Выбор условий регистрации спектров оказывает существенное влияние на результаты спектрофотометрических измерений. [9]
Предположение о существовании двух гидратов указанного состава в растворе кислорода в воде было сделано авторами работы [429] на основе результатов спектрофотометрического измерения коэффициентов адсорбции света растворами кислорода в воде. Приводимые данные по энтальпии образования гидратов рассчитаны из результатов измерения коэффициентов адсорбции и данных по растворимости кислорода в вюде при различных температурах. Какие-либо другие данные, подтверждающие или опровергающие существование гидратов кислорода, в настоящее время неизвестны. [10]
В цитированной выше статье описана методика, основанная на экстрагировании метиловым спиртом и дающая результаты, хорошо согласующиеся с результатами спектрофотометрических измерений. [11]
Для гидроксильных групп характерно сильное поглощение в инфракрасной области, однако при попытках разработать общие количественные методы определения этих групп по результатам прямых спектрофотометрических измерений в этой области спектра возникают определенные трудности. Эти трудности обусловлены тем, что гидроксильные группы могут образовывать между собой и с другими полярными группами водородные связи, влияющие на интенсивности полос поглощения. В отдельных случаях хорошие результаты дают методы, в которых степень ассоциации в системе контролируется путем выбора специальных условий. Выбранные условия обеспечивают либо полную ассоциацию, либо полную диссоциацию, либо определенное соотношение между ассоциированной и неассоциированной частями анализируемой и стандартной систем. Степень межмолекулярной ассоциации зависит от концентрации: сильное разбавление образца неполярными растворителями способствует диссоциации, а разбавление его полярными растворителями, например пиридином, вызывает практически полную ассоциацию. С другой стороны, неполярные растворители не влияют на степень внутримолекулярной ассоциации. [12]
Для гидроксильных групп характерно сильное поглощение в инфракрасной области, однако при попытках разработать общие количественные методы определения этих групп по результатам прямых спектрофотометрических измерений в этой области спектра возникают определенные трудности. Эти трудности обусловлены тем, что гидроксильные группы могут образовывать между собой и с другими полярными группами водородные связи, влияющие па интенсивности полос поглощения. В отдельных случаях хорошие результаты дают методы, в которых степень ассоциации в системе контролируется путем выбора специальных условий. Выбранные условия обеспечивают либо полную ассоциацию, либо полную диссоциацию, либо определенное соотношение между ассоциированной и пеассоциировапной частями анализируемой и стандартной систем. Степень межмолекулярной ассоциации зависит от концентрации: сильное разбавление образца неполяр-ными растворителями способствует диссоциации, а разбавление сто полярными растворителями, например пиридином, вызывает практически полную ассоциацию. С другой стороны, неполярные растворители не влияют на степень внутримолекулярной ассоциации. [13]
Для гидроксильных групп характерно сильное поглощение в инфракрасной области, однако при попытках разработать общие количественные методы определения этих групп по результатам прямых спектрофотометрических измерений в этой области спектра возникают определенные трудности. Эти трудности обусловлены тем, что гидроксильные группы могут образовывать между собой и с другими полярными группами водородные связи, влияющие па интенсивности полос поглощения. В отдельных случаях хорошие результаты дают методы, в которых степень ассоциации в системе контролируется путем выбора специальных условий. Выбранные условия обеспечивают либо полную ассоциацию, либо полную диссоциацию, либо определенное соотношение между ассоциированной и пеассоциировапной частями анализируемой и стандартной систем. Степень межмолекулярной ассоциации зависит от концентрации: сильное разбавление образца неполяр-иыми растворителями способствует диссоциации, а разбавление его полярными растворителями, например пиридином, вызывает практически полную ассоциацию. С другой стороны, неполярные растворители не влияют на степень внутримолекулярной ассоциации. [14]
Спектрофотометрические измерения обеспечивают высокую точность, в определении концентрации поглощающих веществ. Однако результаты спектрофотометрических измерений в растворах кислот ( оснований) и их солей могут быть искажены вследствие изменения электронных спектров поглощения при добавках электролитов и неэлектролитов. Введение в раствор электролитов или неэлектролитов может привести либо к сдвигу полосы поглощения, либо к изменению молярного коэффициента погашения на максимуме полосы. Обычно оба эффекта проявляются одновременно. Они приводят к кажущемуся изменению концентрации поглощающего вещества. В одних случаях наблюдаемый эффект может быть вызван взаимодействием между поглощающим веществом и добавленным с образованием комплексных соединений или ассоциатов. Однако, поскольку аналогичные эффекты наблюдаются и при добавках неэлектролитов, представляется убедительным утверждение [272, 263-267, 270], что они не могут быть объяснены только ионным взаимодействием по теории Дебая - Гюккеля, а причина заключается в изменении взаимодействия между поглощающим ионом и молекулами растворителя, образующими сольватную оболочку. [15]
Страницы: 1 2