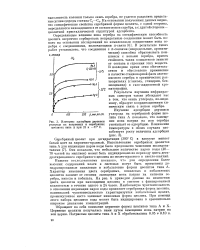
Результат - изучение - инфракрасный спектр
Cтраница 1
Результаты изучения инфракрасных спектров также убеждают нас в том, что окись углерода, по-видимому, образует координационную химическую связь с ионом серебра. [2]
По данным Е. А. Глебовской, результаты изучения инфракрасных спектров показывают резко различный характер кислородных групп в асфальтово-смолистых компонентах рассеянного органического вещества пород и в асфальтово-смолистых компонентах нефтей. [3]
Действительное значение частоты v4 было установлено Арнеттом и Крауфордом [568] в результате изучения инфракрасных спектров молекулы этилена и молекул всех дейтеро-замещенных этилена в области частот неплоских колебаний v4, v7, v8 и последующей теоретической обработки полученных данных. Это позволило достаточно надежно определить силовую постоянную крутильного колебания и вычислить значения v4 молекул С2Н4, цмс - С2Н2О2, СН2 - CD2 и C2D4, в колебательных спектрах которых эта частота неактивна. [4]
Имея в виду способность дитизона к таутомерному превращению, большое сродство металлов, которые образуют дитизонаты, к сере, аналогию между рядами дитизонатов и сульфидов, а также результаты изучения инфракрасных спектров [51], обычно считают [52 - 54], что связь между металлом и реактивом в дитизонатах осуществляется через серу. [5]
В следующих выпусках Справочника будут приведены данные, характеризующие структуру молекул углеводородов ( расстояния между атомами, углы между связями, моменты инерции молекул и частоты колебаний в молекулах углеводородов), познанные, главным образом, в результате изучения Раман-и инфракрасных спектров углеводородов. Эти данные используются далее для подсчета таблиц зависимости от температуры свободных энергий, теплосодержаний, внутренних энергий углеводородов в стандартных состояниях. Далее будут приведены таблицы свободных энергий образования углеводородов из элементов при 25 С, охватывающие более широкий круг соединений, в которых будут также приведены величины, необходимые для приближенного подсчета равновесий реакций между углеводородами. После данных о соотношениях между температурой, давлением и объемом углеводородов будут приведены таблицы летучестей, коэфициентов активности, джоуль-томсоновских коэфициен-тов, теплосодержаний, энтропии и теплот испарения углеводородов под давлением. [6]
Сообщалось [9], что фенилзамещенные фосфорорганиче-ские реагенты склонны к образованию фенольных групп на бензольном кольце в орто-положении к атому фосфора и что указанные реагенты хорошо экстрагируют продукты деления. Однако это противоречит результатам изучения инфракрасных спектров и исследований с помощью радиоактивных индикаторов. [7]
Интерпретация физических данньпх по адсорбционной связи является значительно более полной, чем в случае обычной химической связи. Это относится и к спектроскопическим измерениям ( см., например, результаты изучения инфракрасных спектров Эйшенса с сотрудниками [18]), но в значительно большей степени к определениям магнитных свойств и дипольных моментов. [8]
J ( C ] 0H12 - дицикло-пентадиен) диолефин является хелатным лигандом за счет двух двойных связей. Предположение о том, что этот комплекс является быс - ( л-цикло-пентадиенилом), опровергается наличием сложного поглощения в области частот валентных колебаний СН, а отсутствие поглощения в области валентных колебаний С С рассматривается как указание на то, что обе олефиновые связи координированы с металлом. Чатт, Валларино и Венанци [29] исследовали комплексы платины с дициклопентадиеном и другими диолефинами, у которых пространственное расположение допускает образование хелатных циклов. Они использовали многочисленные химические данные о строении таких соединений и дополнили их результатами изучения инфракрасных спектров, согласующимися с тем, что координация происходит через двойные связи. В то время как дипентен имеет интенсивную полосу при 1674 еж 1, обусловленную валентными колебаниями С С, у комплекса [ Pt ( C10Hie) Cl2 ] есть сильная полоса при 1512 см 1, которую относят к тем же колебаниям, но измененным вследствие координации. Пришлось предположить, что эти две полосы поглощения обусловлены в основном несимметричными концевыми группами Н2С С -, тогда как сравнительно более симметричная группа в цикле приводит к гораздо более слабому поглощению, которое не удается отделить от более сильной полосы. Таким образом, данные по инфракрасным спектрам сами по себе еще не доказывают, что дипентен образует хелатный цикл, но; взятые вместе с химическими данными, они хорошо согласуются с таким заключением. [9]
Как уже упоминалось, молекулы в кристалле колеблются около центров равновесия. При этом жесткие молекулы низкомолекулярных ароматических соединений колеблются как единое целое, а для цепных молекул, например для полиэтилена, возможно колебание отдельных участков молекулы. Таким образом, последние имеют значительно большее число степеней свободы. Поэтому можно допустить, что в первом случае для плавления требуется большая энергия, чем для цепных молекул. Такой вывод вытекает также из результатов изучения инфракрасных спектров. [10]
Страницы: 1