Значение - общее давление
Cтраница 1
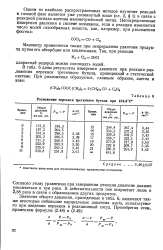 |
Разложение перекиси третичного бутила при 154 6 С. [1] |
Значения общего давления, приведенные в табл. 6, включают также некоторые небольшие парциальные давления азота, используемого при введении перекиси в реакционный сосуд. [2]
В табл. 7 приведены значения общего давления в системе в различные моменты времени, начиная от известного начального давления акролеина и бутадиена. На основании этих данных для каждого последующего интервала времени вычислены изменения давления акролеина и бутадиена. Сделано это следующим образом. [3]
В табл. 11 приведены значения общего давления над жидкостью, найденные путем непосредственного замера по манометру, парциальные давления NH3, CO2 и Н2О, определенные путем весового анализа, и суммарное давление, подсчитанное как сумма парциальных давлений. [4]
На оси ординат откладывается значение общего давления Р и проводится горизонтальная линия. Точка С определяет максимальную температуру процесса tz, когда давление водяного пара равно нулю. При наименьшей температуре процесс идет с насыщенным водяным паром. Необходимо отметить, что водяной пар, подведенный из котла, может быть насыщенным, но когда процесс идет при температуре выше ti, то водяной пар в летучей смеси будет ненасыщенным. [5]
На оси ординат откладывается значение общего давления Р и проводится горизонтальная линия. Точка С определяет максимальную температуру процесса tz, когда давление водяного пара равно нулю. Затем параллельно линии давления насыщенного пара жидкости проводится линия АВ. При наименьшей температуре процесс идет с насыщенным водяным паром. Необходимо отметить, что водяной пар, подведенный из котла, может быть насыщенным, но когда процесс идет при температуре выше tt, то водяной пар в летучей смеси будет ненасыщенным. [6]
Данные различных исследователей о значении общего давления паров над олеумом расходятся. [7]
В табл. 2 приведены парциальные давления, а также значения общего давления над растворами нитрита аммония. [8]
Нетрудно констатировать, что транспорт в простых ампулах при значениях общего давления от 0 2 до 4 ат можно рассчитать без большой ошибки, если предположить наличие диффузии между двумя равновесными зонами. Даже при 2Р 0 01 ат результат расчета Q 0 27 представляет собой еще вполне удовлетворительное приближение. [9]
Нетрудно констатировать, что транспорт в простых ампулах при значениях общего давления от 0 2 до 4 ат можно рассчитать без большой ошибки, если предположить наличие диффузии между двумя равновесными зонами. Даже при 2Р 0 01 ат результат расчета Q 0 27 представляет собой еще вполне удовлетворительное приближение. [10]
Нетрудно констатировать, что транспорт в простых ампулах при значениях общего давления от 0 2 до 4 ат можно рассчитать без большой ошибки, если предположить наличие диффузии между двумя равновесными зонами. Даже при 2Р 0 01 ат результат расчета Q 0 27 представляет собой еще вполне удовлетворительное приближение. При еще меньших давлениях скорость реакции становится совсем незначительной. [11]
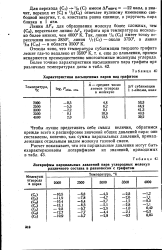 |
Характеристика насыщенных паров над графитом. [12] |
Чтобы лучше представить себе смысл величин, обратимся прежде всего к расшифровке значений общих давлений пара: они составлены, конечно, как сумма парциальных давлений, принадлежащих отдельным видам молекул газовой смеси. [13]
В общих чертах расчетная схема основана на определении параметров уравнения Вильсона, удовлетворяющего дифференциальному уравнению Гиббса - Дюгема, путем минимизации отклонения между расчетным и экспериментальным значениями общего давления. [14]
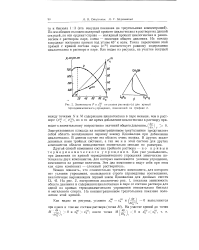 |
Зависимость Р и х от состава раствора ( а для кривой термодинамического упрощения, показанной на графике б. [15] |
Страницы: 1 2