Результат - кинетический расчет
Cтраница 1
Результаты кинетических расчетов сравнены с экспериментальными данными. [1]
Результаты подобных кинетических расчетов для воздуха, находившегося вначале в равновесном состоянии при 7000 К и 1 атм, температура которого снижалась по закономерностям, показанным на рис. VII.4, иллюстрируются графиками рис. VII.5. Состав газа в любой момент процесса закалки зависит от температуры газа в тот же момент времени. [2]
Из результатов кинетического расчета видно, что энергия активаций процесса образования волокнистого углеродного вещества очень мала для Ланйой области температур. Процесс образования волокнистого углеродного вещества в области температур 400 - 500 С лимитируется диффузионными факторами, вызванн ы мй транспортом вещества к поверхности катализатора и транспортов Нро дуктов реакции с поверхности катализатора или другими фактораМй, специфичными для дендритного механизма. [3]
Более детальный анализ результатов кинетического расчета позволяет проследить также за особенностями многокомпонентной массопередачи при ректификации смесей в многотарельчатом аппарате. [4]
Как видно из таблицы, наблюдается удовлетворительное совпадение результатов термодинамических и кинетических расчетов, что может служить подтверждением приемлемости выбранного механизма процесса. [5]
Экспериментальные данные по термоокислителыюму пиролизу этилена удовлетворительно согласуются с результатами кинетических расчетов. Полученные данные-по пиролизу этана, пропана и бутана подтверждают представление, в соответствии с которым определяющими реакциями в механизме пиролиза этих углеводородов до ацетилена являются реакции разложения метана и этилена. [6]
 |
Зависимость кинетических характеристик от температуры ведения процесса. [7] |
Кинетические характеристики для процесса, протекающего в области температур 400 - 600 С, совпадают с литературными данными95 101 102 для процессов углеродообразования, протекающих по дендритному механизму. Из результатов кинетического расчета видно, что энергия активации процесса образования волокнистого углеродного вещества очень мала для данной области температур. [8]
Сопоставление результатов кинетических расчетов для коротких цепей, проведенных без каких-либо допущений и с допущением (111.23), показало [15], что это допущение не вносит существенной ошибки. При изучении обратимых процессов наибольший интерес всегда представляет рассмотрение состояния равновесия. [9]
Как указывалось выше, при анализе результатов, полученных хро-матографическими методами, следует учитывать, что катализатор в промежутках между импульсами подвергается частичной регенерации потоком газа-носителя, вследствие чего стационарное состояние катализатора может и не достигаться. В принципе, результаты кинетических расчетов, полученные на основе хроматографических данных, могут отличаться от констант, соответствующих стационарному состоянию катализатора ( см., например, стр. Хроматографические данные представляют значительный интерес, поскольку они характеризуют наиболее активные в каталитическом отношении центры поверхности. Сопоставление результатов, полученных в хроматографических условиях, с результатами, полученными в проточных и проточно-циркуляционных системах, может дать дополнительно существенную информацию о кинетике и механизме каталитического процесса. Мы уже указывали выше, что эффективность кинетических исследований значительно повышается при проведении опытов по определенной стратегии. Этому вопросу посвящен специальный раздел математической статистики, называемый планирование экстремальных экспериментов. [10]
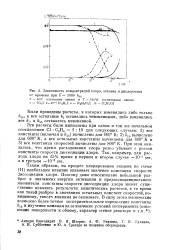 |
Зависимость концентраций хлора, этилена И дихлорэтана от времени при к 1000 к1ъ. [11] |
Таким образом, на процесс хлорирования этилена по схеме ( 11) наибольшее влияние оказывает значение константы скорости диссоциации хлора. Поэтому даже относительно небольшой разброс в значениях энергии активации и предэкспоненциального множителя константы скорости диссоциации хлора может существенно исказить результаты кинетических расчетов, в то время как такой разброс в значениях остальных констант скоростей, по-видимому, такого влияния не оказывает. [12]
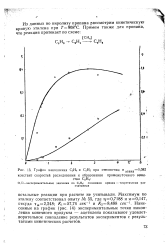 |
График накопления С2Н4 и С2Н2 при отношении х 0 082. [13] |
Нанесенные на график ( рис. 14) экспериментальные точки накопления конечного продукта - ацетилена показывают удовлетворительное совпадение результатов экспериментов с результатами кинетических расчетов. [14]
Страницы: 1