Результат - титрование
Cтраница 1
Результаты титрования нескольких проб приведены в таблице. [1]
Результаты титрования приведены в табл. 2 и на фиг. [2]
Результаты титрования позволяют определять константы диссоциации слабых кислот и оснований, в том числе полифункциональных. По этой причине потенциометрический метод является одним из важнейших методов изучения полиэлектролитов, в том числе и биополимеров, таких как белки, полипептиды, нуклеиновые кислоты. [3]
Результаты титрования будут правильными, если в конце титрования окраска титруемого раствора резко изменится от одной капли рабочего раствора. [4]
Результаты титрования 0 1 М NaCl раствором AgNOa приведены на рис. 3, из которого видно, что кривые титрования с аннонитовыми мембранными электродами совпадают по характеру изменения ЭДС с кривой титрования с хлорсеребряным электродом. В эквивалентной точке наблюдается достаточно резкий скачок потенциала. Кривая титрования, приведенная на рис. 4, показывает, что в эквивалентных точках, соответствующих полному осаждению галогенида, имеются четко выраженные скачки. [5]
Результат титрования записывают по принятой форме. [6]
Результаты титрования записывают по принятой форме. [7]
Результаты титрования более точны в присутствии смешанного индикатора; в качестве такового можно применять смесь равных частей 0 1-процентного спиртового раствора диметилового желтого и 0 1-процентного спиртового раствора метиленового синего. Титруют до перехода окраски в сине-фиолетовый цвет. [8]
Результат титрования получается хорошим, когда во взятом объеме воды будет находиться не более 0 5 мг-экв ионов кальция и магния. Поэтому в зависимости от ожидаемой жесткости необходимо брать следующие объемы проб исследуемой воды: для воды с жесткостью от 0 5 до 5 0 мг-экв / л - 50 мл; от 5 0 до 10 0 мг-экв / л - 25 мл; от 10 0 до 50 0 мг-экв / л - 10 мл. [9]
Результат титрования получается хорошим, когда во взятом объеме воды будет находиться не более 0 5 мг-экв ионов кальция и магния. [10]
Результаты титрования записываются в таблицу. [11]
Результат титрования не зависит от температуры раствора. [12]
Результаты титрования представлены в таблице и на рисунке. Величины соответствующих констант иона [ Ptm4I4H3Cl ] 3 рассчитывались по формулам для одноосновных кислот, а для иона [ Pt ( NH3) 5Cl ] 3 получены из формул для двухосновных кислот. [13]
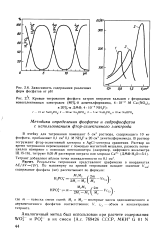 |
Зависимость содержания различных форм фосфатов от рН.| Кривые титрования фосфата натрия нитратом кальция с фторидным. [14] |
Результаты титрования представляют графически в координатах А. [15]
Страницы: 1 2 3 4