Атомный вес
Cтраница 2
Атомный вес 195 09, плотность 21 4 - г / см, температура плавления 1773 С, температура кипения 4180 С. [16]
Атомный вес 180 95, плотность 16 6 - г / ел, температура плавления 2850 С. [17]
Атомный вес, с которым имеет дело химик, есть вес смеси изотопов, и он не столь уж существен. Сейчас известны ведь и изобары - атомы одинакового веса, но с рааным числом электродов, следовательно, атомы разных химических элементов. Например, изотоп аргона с массовым числом ( атомным весом) 40, содержащий 18 протонов и 22 нейтрона, и изотоп калия с тем же массовым числом, содержащий 19 протонов и 21 нейтрон. [18]
Атомный вес, с которым имеет дело химик, есть вес смеси изотопов, и он не столь уж существен. Сейчас известны ведь и изобары - атомы одинакового веса, но с разным числом электронов, следовательно, атомы разных химических элементов. Например, изотоп аргона с массовым числом ( атомным весом) 40, содержащий 18 протонов и 22 нейтрона, и изотоп калия с тем же массовым числом, содержащий 19 протонов и 21 нейтрон. [19]
Атомный вес показывает, во сколько раз атом данного элемента тяжелее одной кислородной единицы. Соответственно и молекулярным весом вещества называется вес его молекулы, выраженный в кислородных единицах. [20]
 |
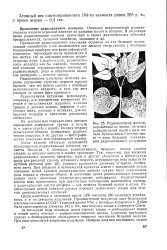
Схема различных изотопов атомов лития. Большие круги - ядра атомов, . маленькие - протоны ( с знаком - f и нейтроны. А-атомный вес изотопа, Z-порядковый номер. [21] |
Атомный вес равен числу протонов и нейтронов. [22]
Атомный вес - число, выражающее массу 1 атома элемента в углеродных единицах. [23]
Атомный вес - это число, показывающее, во сколько раз масса атома данного элемента больше / is массы атома кислорода. [24]
Атомный вес - одна из величин, наиболее характерная для химического элемента. Это понятие было введено в науку английским ученым Дж. [25]
 |
Радиоавтограф фасоли, выращенной иг семян, меченых радиоактивной серой в фазе начала бутонизации. Светлые места - зоны большой локализации радиоактивного излучения. [26] |
Атомный вес синтезированного 104-го элемента равен 260 у. [27]
Атомный вес - число, выражающее массу 1 атома данного моноизотопического элемента или же среднюю массу атома плеяды элемента ( если последний полиизотопичен), в углеродных единицах. [28]
Атомный вес принадлежит не углю и алмазу, ауглороду ( стр. [29]
Атомный вес принадлежит не углю и алмазу, а углероду. Способ, которым Жерар и Канницаро определили атомные веса элементов, основывается на таких незыблемых и несомненных приемах, что для большинства тел, в особенности для тех простых тел, которых теплоемкость в свободном состоянии уже определена, нет сомнения в атомном весе элемента, как это было несколько лет тому назад, когда атомный вес столь часто смешивался с эквивалентом и определялся на основании разнородных, часто противуположных начал. [30]
Страницы: 1 2 3 4