Металлический рений
Cтраница 2
Металлический рений взаимодействует с фтором и хлором при нагревании до 100 С, с бромом - выше 300 С, а с иодом рений в реакции не вступает. При сильном нагревании рений реагирует и со всеми остальными неметаллами. Технеций в этом отношении подобен рению. [16]
Металлический рений, как показано в работе [489], выделяется на электроде лишь при концентрациях рения в растворах и плотностях тока, во много раз превышающих их значения в полярографических исследованиях, а также при более отрицательных потенциалах. [17]
 |
Взаимное расположение компонент аналитической линии рения и линий мешающих элементов ( спектрограф ДФС-13, дисперсии. [18] |
Металлический рений принадлежит к числу наименее летучих металлов и вместе с W, Mo, Та, Nd, Zr, lif и Th располагается в конце ряда летучести свободных элементов в угольной дуге. Рений испаряется крайне медленно. [19]
Металлический рений, полученный из перрепатов калия и аммония, или крупные куски рениевого лома помещают в никоровую трубку, через которую пропускают водород при температуре 1000 для полного восстановления окислов металла. Затем систему охлаждают до 750 в токе гелия и выдерживают при этой температуре в течение 1 час для удаления водорода. После этого вместо гелия пропускают хлор; при небольшом давлении хлора рений переводится в ReCls, который возгоняется из реакционной зоны и конденсируется в охлаждаемой воздухом ловушке. В указанных условиях образуется примерно 150 г ReQU в 1 час. [20]
Металлический рений, нанесенный на пластинки из платины, серебра, тантала, меди и латуни, сохраняет сильный блеск до тех пор, пока образцы находятся в совершенно сухой атмосфере. Леви и Эсперсен [ 461 нашли, что, если рениевое покрытие на вольфрамовой нити сразу же после нанесения нагревать до 1000 в атмосфере водорода, оно будет устойчивым во влажном воздухе при комнатной температуре в течение длительного времени. [21]
Металлический рений, образующийся при восстановлевии KReO4 или NaReO4 в аналогичных условиях, всегда содержит до 1 % соединений калия или натрия. [22]
Металлический рений взаимодействует с фтором и хлором при нагревании до 100 С, с бромом - выше 300 С, а с иодом рений в реакции не вступает. При сильном нагревании рений реагирует и со всеми остальными неметаллами. Технеций в этом отношении подобен рению. [23]
Металлический рений, полученный электролитически, всегда насыщен водородом, который может быть удален прокаливанием металла в вакууме. При прокаливании снимаются также напряжения, возникающие в металле при электролитическом его отложении [65], благодаря чему устраняется хрупкость металла. [24]
Металлический рений может быть получен восстановлением водородом из окислов, галогенидов, сульфидов или перренатов. Восстановление галогенидов и перренатов идет легко при 250 - 500 С; восстановление окислов происходит при более высоких температурах. [25]
Металлический рений получают также электролизом водных растворов перрената калия. Этот процесс рассмотрен выше в разделе об электрохимических свойствах рения. [26]
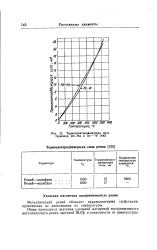 |
Термоэлектродвижущая сила термопар Re-Мо и Re - W. [27] |
Металлический рений обладает парамагнитными свойствами, практически не зависящими от температуры. [28]
Металлический рений чаще всего получают восстановлением перренатов калия или аммония водородом. [29]
Металлический рений и его сплавы обладают уникальными физико-химическими свойствами, что обеспечивает их применение в важнейших областях современной техники. Высокая температура плавления рения ( 3180 С) и замечательные механические свойства при высоких температурах обеспечили его применение в производстве жаропрочных сплавов, а малая упругость паров при этих температурах и высокое удельное сопротивление ( 2 1 - 10 - 5ом - см) дает возможность широкого применения его в электронной технике. Сплавы рения с платиновыми элементами и вольфрамом используются для изготовления термопар, работающих при температурах свыше 2000 С, благодаря высокой термоэлектродвижущей силе при этих температурах. Коррозионная устойчивость рения по отношению к агрессивным средам ( газообразный хлористый водород, его растворы и др.) позволяет применять его в качестве покрытий для защиты ряда металлов. [30]
Страницы: 1 2 3 4