Низкое значение - энергия - ионизация
Cтраница 1
Низкие значения энергии ионизации характеризуют высокую восстановительную активность щелочных металлов. [1]
Их атомы имеют самые низкие значения энергии ионизации. Атомы этих элементов обладают наивысшими значениями сродства к электрону. [2]
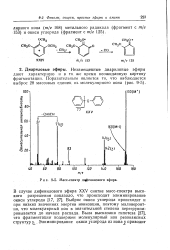 |
Масс-спектр дцфенилового эфира. [3] |
Выброс окиси углерода происходит и при низких значениях энергии ионизации, поэтому маловероятно, что молекулярный ион в значительной степени перегруппировывается до начала распада. [4]
Восстановительная активность металлов возрастает от Li к Fr, что обусловлено увеличением радиусов атомов в этом направлении и низкими значениями энергий ионизации. [5]
Такая склонность к отдаче электронов этими металлами и превращению в водных растворах в положительные ионы объясняется тем, что валентные электроны их атомов не очень прочно связаны с атомным ядром, о чем свидетельствуют низкие значения энергии ионизации. [6]
Их высокая химическая активность обусловлена в первую очередь низкими значениями энергии ионизации их атомов - легкостью отдачи ими валентных электронов. Ясно, что химическая активность при этом возрастает. [7]
Их высокая химическая активность обусловлена в первую очередь низкими значениями энергии ионизации их атомов - легкостью отдачи ими валентных электронов. Ясно, что восстановительная активность при этом возрастает. [8]
Их высокая химическая активность обусловлена в первую очередь низкими значениями энергии ионизации их атомов - легкостью отдачи ими валентных электронов. Ясно, что химическая активность при этом возрастает. [9]
Их высокая химическая активность обусловлена в первую очередь низкими значениями энергии ионизации их атомов - легкостью отдачи ими валентных электронов. Ясно, что химическая активность при этом возрастает. [10]
Их высокая химическая, активность обусловлена в первую очередь низкими значениями энергии ионизации их атомов - легкостью отдачи ими валентных электронов. Ясно, что химическая активность при этом возрастает. [11]
На внешнем энергетическом уровне атомов этих элементов имеется один s - электрон, который они при химических реакциях легко отдают другим атомам. Значительная величина радиуса атомов ( от 1 57 у Li до 2 62 А у Cs) и низкие значения энергии ионизации ( от 5 39 эв у Li до 3 89 эв у Cs) характеризуют эти элементы как очень активные восстановители. [12]
Теперь, когда мы немного разобрались, почему меняется прочность связи валентных электронов с ядром в зависимости от положения элемента в Периодической системе, то овладели аппаратом, который позволит понять разделение простых веществ на металлы и неметаллы. Повторим, что нам известно о металлах. Их отличает металлический блеск, высокая тепло - и электропроводность, прочность и пластичность. Атомы металлов имеют низкие значения энергии ионизации. Их электроотрицательность тоже относительно невелика. Как связаны эти свойства со строением. [13]
Страницы: 1