Структурный аналог
Cтраница 3
Рассматриваемые тритиофосфиты являются структурными аналогами средних фосфитов, в связи с этим они обладают некоторыми одинаковыми с ними свойствами. В то же время фосфиты и тиофосфиты резко различаются между собой во многих химических реакциях, что объясняется своеобразием строения электронной оболочки серы по сравнению с оболочкой кислорода, в частности с наличием у серы вакантных 3d орби-талей. [31]
Жабы А1е1ори спшдшоша продуцируют структурный аналог тетродртоксина - чирикитотоксин ( содержит не-идентифицир. Блокирует также К-каналы возбудимых мембран. [32]
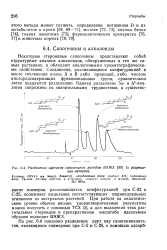 |
Разделение ацетатов сапогенинов методом ВЭЖХ ( с разрешения авторов. [33] |
Некоторые стероидные сапогенины представляют собой структурные аналоги алкалоидов, обнаруженных в тех же самых растениях, и обладают аналогичными хроматографически-ми свойствами. Соединения, различающиеся конфигурацией в месте сочленения колец А и В либо природой, либо числом кислородсодержащих функциональных групп, сравнительно легко поддаются разделению. [34]
В медицине широко используются структурные аналоги парааминобензойной кислоты, в частности сульфаниламиды, обладающие антибактериальными свойствами. Предполагают, что сульфаниламидные препараты вследствие структурного сходства могут конкурентно замещать парааминобензойную кислоту в ферментных системах микроорганизмов с последующей остановкой их роста и размножения. Коферментные функции этой кислоты не установлены, но, являясь составной частью ко-ферментов фолиевой кислоты, Парааминобензойная кислота тем самым участвует во многих процессах обмена. [35]
Полисахарид хитин, являющийся структурным аналогом целлюлозы, так же распространен в природе, как целлюлоза. [36]
Поскольку ДФФ не является полным структурным аналогом нормальных субстратов этих ферментов, опасность присоединения метки не к активному центру, а к каким-то другим участкам молекулы фермента в этом случае, естественно, больше, нежели в случаях, описанных выше. Однако скорость, стехиометрия и специфичность реакции присоединения ДФФ явно указывают, что метка действительно попадает в активный центр. Известно, например, что ДФФ специфически фосфорилирует один из двух остатков серина в химотрипсине. Химотрипсин может быть помечен и многими другими аналогичными агентами, в том числе и-нитрофенилацетатом, причем в каждом случае ацилируется одна и та же гидроксильная группа серина, тогда как никакие другие группы не ацилируются. Во многих ( хотя и не во всех) исследованных эстеразах и протеиназах ДФФ фосфорилирует гидроксиль-ную группу только того серина, с N-концом которого связан либо аланин, либо глицин. Из таблицы видно, что даже ферменты, сильно различающиеся по своей специфичности, могут иметь одинаковую последовательность аминокислот в участках, примыкающих к остатку серина, содержащему реакционноспособную гидроксильную группу. [37]
Вновь синтезированные азот - и серусодержащие структурные аналоги ионола способны тормозить реакцию окисления не только в период ее зарождения, но и в стадии ее развития. Это определяется как их способностью вступать во взаимодействие с первичными радикалами окисляемого вещества, так и способностью разрушать перекиси и связывать ионы металлов переменной валентности. [38]
Вновь синтезированные азот - и серусодержащие структурные аналоги ионола способны тормозить реакцию окисления не только в период ее зарождения, но и в стадии ее развития. Это определяется как Их способностью вступать во взаимодействие с первичными радикалами окисляемого вещества, так и способностью разрушать перекиси и связывать ионы металлов переменной валентности. [39]
Кристаллические фазы системы интересны как структурные аналоги типичных силикатных фаз. [40]
 |
Диаграмма состояния системы SrO - Ge02. [41] |
Кристаллические фазы системы интересны как структурные аналоги соответствующих силикатных фаз. [42]
Эта перегруппировка типична для всех структурных аналогов гидразобензо-ла, содержащих в пора-положениях фенильных групп или атомы водорода или функциональные группы, способные покидать молекулу в условиях реакции. [43]
По-видимому, соединения, являющиеся структурными аналогами и различающиеся между собой только степенью ненасыщенности, биогенетически родственны и их образование в растениях можно рассматривать как результат биохимического превращения общих предшественников. В этом отношении интересно отметить синтез в Artemisia selengensis двух вторичных спиртов. Триин-еновый спирт CLVII имеет по данным ИК-сцектра тераке-конфи-гурацию двойной связи и конечную винильную группу. [44]
Энпиролин ( 72) является структурным аналогом хинина и проявляет токсическое действие против плазмодиев - микроорганизмов, вызывающих малярию. При синтезе энпиролина ненасыщенную кетокислоту ( 67) конденсируют с трифторацетил-метилпиридинийбромидом ( 68) и ацетатом аммония. Последний каталитически гидрируют в уксусной кислоте и получают диастереомерную смесь энпиролина ( 72) Селективность восстановления связана со значительно большей стерической доступностью неподеленной электронной пары азота в монозамещенном пиридиновом ядре к протонированию и отсутствием в нем электроноакцепторных заместителей. [45]
Страницы: 1 2 3 4