Кристаллическая решетка - тип - алмаз
Cтраница 1
Кристаллическая решетка типа алмаза, которой обладают германий и кремний, представлена на рис. 1 а. [1]
Система железо - кремний ( фиг 8) Кремнии обладает кристаллической решеткой типа алмаза. Незначительная температурная зависимость растворимости обусловливает малую склонность этих сплавов к дисперсионному твердению. [2]
Полупроводниковыми свойствами обладает только модификация серого олова a - Sn с кристаллической решеткой типа алмаза. Скорость перехода обычного белого олова ( З - Sn в серое увеличивается с повышением его чистоты, особенно в интервале температур ( - 10) - - ( - 30) С. Ширина запрещенной зоны серого олова равна примерно 0 082 эв. [3]
Подобная тенденция прослеживается и в изоэлектронном ряду кремния: у самого кремния кристаллическая решетка типа алмаза, у А1Р - кубическая ( сфалерит), а уже у MgS и, тем более, у NaCl реализуется ионная решетка с к. Различие между структурами вертикальных изоэлектронных аналогов ВеО и MgS определяется большей ионностью связи в последнем. [4]
Изменение свойств полупроводников под действием примесей удобно рассмотреть на примере германия, имеющего кристаллическую решетку типа алмаза. Энергетические зоны германия аналогичны зонам алмаза, только имеют другую ширину. [5]
Олово существует в двух полиморфных модификациях, причем низкотемпературная ( o - Sn - серое олово) обладает кристаллической решеткой типа алмаза и полупроводниковыми свойствами, а высокотемпературная ( fi - Sn - белое олово), хотя и представляет собой металл по физическим свойствам, тем не менее кристаллизуется в малохарактерной для металлов тетрагональной структуре. С хими-ческой точки зрения, олово ближе примыкает к германию, чем к свинцу, но металлический характер этого элемента выражен более ярко, чем у германия. Единственным типичным металлом в этой подгруппе является свинец. В своих соединениях он выступает в основном в качестве катионообразователя. [6]
Олово существует в двух полиморфных модификациях, причем низкотемпературная ( a - Sn - серое олово) обладает кристаллической решеткой типа алмаза и полупроводниковыми свойствами, а высокотемпературная ( fi - Sn - белое олово), хотя и представляет собой металл по физическим свойствам, тем не менее кристаллизуется в малохарактерной для металлов тетрагональной структуре. С химической точки зрения олово ближе примыкает к германию, чем к свинцу, но металлический характер этого элемента выражен более ярко, чем у германия. Единственным типичным металлом в этой подгруппе является свинец. В своих соединениях он выступает в основном в качестве катионообразователя. [7]
Они имеют кристаллическую решетку типа алмаза. [8]
Полупроводники образуют сложные кристаллы. Германий и кремний имеют кристаллическую решетку типа алмаза. Координационное число здесь равно четырем. Селен и теллур имеют гексагональные решетки; бор может существовать в виде нескольких кристаллических модификаций. [9]
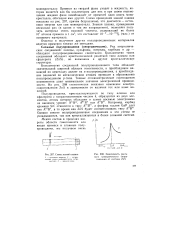 |
Схема зонной плавки.| Зависимость удельного электрического сопротивления от состава ZnS. [10] |
Ряд неорганических соединений: оксиды, сульфиды, нитриды, карбиды и др. - обладают полупроводниковыми свойствами. Большинство таких соединений обладает кристаллической решеткой типа алмаза или сфалерита ( ZnS), но возможны и другие кристаллические структуры. [11]
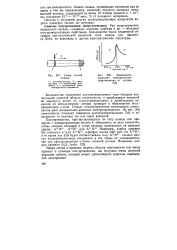 |
Схема зонной плавки. [12] |
Ряд неорганических соединений: оксиды, сульфиды, нитриды, карбиды и др. - обладают полупроводниковыми свойствами. Большинство таких соединений обладают кристаллической решеткой типа алмаза или сфалерита ( ZnS), но возможны и другие кристаллические структуры. [13]
 |
Расположение энергетических.| Кристаллическая структура типа алмазной решетки. [14] |
Германий и кремний обладают валентностью четыре и поэтому химические связи у них могут образовывать четыре электрона. Атомы этих полупроводников группируются в кристаллическую решетку типа алмаза, часть которой представлена в двух измерениях на рис. 8 - 2, а. Каждый из внешних валентных электронов связан ковалентной связью с четырьмя соседними атомами германия. Такого рода ковалент-ная связь является одной из наиболее прочных химических связей и представляет собой очень устойчивое соединение. Для данного случая проводимость может иметь место только при разрыве ковалентных связей; это эквивалентно такому возбуждению электрона, при котором он переходит из валентной зоны в проводящую. [15]
Страницы: 1 2 3