Роль - катализатор
Cтраница 1
Роль катализаторов в процессах восстановления заключается в активировании нитрососдинепия, нитрозосоединения и молекулярного водорода. Последний, как известно, в отсутствие катализатора как восстановитель не действует. [1]
Роль катализаторов особенно велика, если учесть, что из всего разнообразия энергетически возможных реакций они могут избирательно проводить только некоторые из них и осуществлять процесс при более низкой температуре. [2]
Роль катализатора и механизм реакции при каталитическом гидрировании и дегидрировании иные, чем в ранее рассмотренных карбониево-ионных реакциях изомеризации терпенов. Они хорошо объясняются мультиплетной теорией катализа А. [3]
Роль катализаторов в химическом производстве исключительно велика. Получение серной кислоты, аммиака, жидкого топлива, искусственного каучука, пластмасс, гидрогенизация жиров, переработка нефти и природного газа, - вот далеко не полный перечень важнейших производств, где применяются катализаторы. Очевидно, поиски новых, все более совершенных катализаторов будут способствовать повышению производительности труда и снижению себестоимости продукции. [4]
Роль катализатора сводится к тому, чтобы изменить соотношение скоростей реакций образования полезного продукта и разложения его в пользу реакции образования. В этом случае структура пор иногда может оказывать значительное влияние на выходы полезного продукта, снижая их почти вдвое. [5]
Роль катализатора при хлорировании дихлорэтана, Отч. [6]
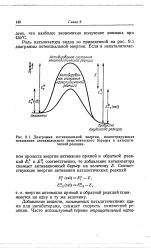 |
Диаграмма потенциальной энергии, иллюстрирующая понижение активационного энергетического барьера в каталитической реакции. [7] |
Роль катализатора видна из приведенной на рис. 9.1 диаграммы потенциальной энергии. [8]
Роль катализаторов особенно велика потому, что они позволяют проводить многостадийные процессы как бы в одну стадию и в заданном направлении при более низких температурах, что дает экономию энергии и времени и подавляет вторичные процессы, снижающие выходы основных продуктов. [9]
Роль катализатора в растворах могут играть растворители, особенно вода, ионы водорода и гидроксид-ионы. Катализ ионами Н и ОН называют кислотно-основным. [10]
Роль катализатора и спиртов как средств повышения предельного выхода заключается в блокировке вредных примесей. Возможно, это связано со способностью спиртов давать относительно малоактивные радикалы и со свойствами катализатора как слабого радикала. [11]
Роль катализатора в данном случае заключается в том, что адсорбируя молекулы алкинов и водорода, металл превращает и те, и другие в радикалы, которые и реагируют между собой. [12]
Роль катализатора не вполне ясна и может быть различной в разных случаях. В таком случае, конечно, реакция будет идти как согласованный [25 28] - процесс. [13]
Роль катализатора не совсем ясна, хотя и было высказано много предположений. Несмотря на то что механизм, как было показано выше, включает свободный карбен и имеется много доказательств в пользу этого [162], возможно также, что в некоторых случаях свободный карбен отсутствует и две стадии реакции совмещаются. [14]
Роль катализатора сводится к генерированию таких поверхностных радикалов. Они генерируются за счет свободных валентностей катализатора, присутствующих на поверхности или возникающих в процессе протекания реакции. [15]
Страницы: 1 2 3 4