Роль - окислитель
Cтраница 2
При этом роль окислителя выполняет вода, а комплексообразующей среды - ОН - ионы. [16]
Выступая в роли окислителя в водном растворе, КМпО4 восстанавливается по-разному в зависимости от реакции среды. [17]
При этом роль окислителя выполняет вода, а комплексообразующей среды - ОН - - ионы. [18]
На пожарах роль окислителя при горении чаще всего выполняет кислород воздуха, окружающего зону протекания химических реакций, поэтому интенсивность горения определяется не скоростью протекания этих реакций, а скоростью поступления кислорода из окружающей среды в зону горения. [19]
Применяют в роли окислителя. [20]
Вследствие этого роль окислителей могут играть разнообразные соединения, главным образом неорганические, реже органические, например, нитросоединения, способные принимать на себя электроны за счет восстановления входящих в их состав атомов, имеющих высшую валентность. [21]
Следовательно, роль окислителя заключается в присоединении электройов, отнимаемых у окисляющегося вещества. [22]
В таких составах роль окислителя выполняет хлорорганиче-ское соединение, горючим является порошок активного металла. [23]
В этом случае роль окислителя играют катионы водорода Н серной кислоты. На медь, серебро, золото и платину ( стоящие в ряду стандартных электродных потенциалов после водорода) разбавленная серная кислота не действует. [24]
Вещества, играющие роль окислителя по отношению к ионам иода, отнимая электроны от ионов 1 - -, окисляют последние до свободного иода, который и будет в этом случае выделяться. [25]
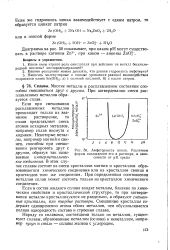 |
Амфотерность цинка. Различные формы нахождения его в растворе, в зависимости от рН среды. [26] |
Какие ионы играют роль окислителя при действии на металл бескислородной кислоты. [27]
В первом случае роль окислителя принимают на себя ионы Н кислот. Так ведут себя соляная, уксусная, разбавленная серная кислоты. [28]
Атомы О играют роль окислителя в реакциях молекулярного кислорода, для которого степень окисления обоих атомов строго равна нулю, поскольку молекула симметрична и совершенно непо-лярна. В этой молекуле степень окисления кислорода равна - 1, так как каждый атом получает по одному электрону от связанного с ним атома Н, а связь О - О неполярна. Занимая по степени окисления кислорода промежуточное положение между молекулярным кислородом и обычными оксидами и их производными, в которых степень окисления кислорода - 2, пероксид водорода может быть как окислителем, так и восстановителем. [29]
Какой элемент играет роль окислителя при сгорании магния в диоксиде углерода. [30]
Страницы: 1 2 3