Роль - перекись
Cтраница 1
Роль перекисей в цепных процессах весьма велика. Они не только являются промежуточными продуктами при цепных реакциях окисления, но и сами по себе способны создавать реакционные цепи. Благодаря пониженному значению энергии связи О-О, составляющему около 50 000 кал, перекиси яеляются мощными. [1]
Выяснению роли перекисей в упомянутых реакциях в значительной степени способствуют исследования кинетики и механизма взаимодействия перекисей с соединениями различных классов. Одним из классов соединений, легко вступающих в реакции с перекисями, являются амины. Интерес к аминам оправдывается еще и тем, что они часто входят в состав комбинированных инициаторов полимеризацион-ных процессов. [2]
Далее была показана роль перекисей не только как промежуточных соединений, но прежде всего как агентов ускорения низкотемпературных реакций; наряду с этим установлена роль альдегидов в ускорении высокотемпературных реакций. [3]
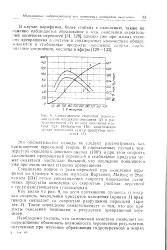
Специально вопрос о роли перекисей при окислении парафинов на примере - декана изучался Вартанян, Майзус и Эмануэлем [134] путем сопоставления скорости накопления устойчивых продуктов окисления со скоростью распада перекисей в среде окисляющегося углеводорода. [5]
Таким образом, исследование роли перекисей при окислении приводит нас к выводу, что образование гидроперекисей в качестве молекулярного промежуточного продукта окисления определяет весь дальнейший ход процесса. [6]
Майзус в кинетическом аспекте анализирует вопрос о роли перекисей в процессах жидкофазного окисления. Собранные в этой работе факты свидетельствуют о том, что скорость низкотемпературного жидко-фазного окислещш углеводородов определяется скоростью распада промежуточных пв р исных соединений. Если элементарные реакции, составляющие химический механизм цепных реакций в газовой фазе, в ряде случаев установлены и изучены, то для жидкофазных реакций окисления эта работа еще только начинается. [7]
По нашему мнению, имеющийся в настоящее время фактический материал относительно роли перекисей в химии живых клеток позволяет высказать следующие гипотезы. [8]
Норриш и Брокман [ 107а ] и Медведев и Каменская [1076] объясняют роль перекисей как ускорителей полимеризации их распадом с образованием свободных радикалов. [9]
Мы уже касались вопроса об образовании окислов углерода в связи с исследованием роли перекисей, альдегидов и спиртов в окислении углеводородов. Это серьезный пробел, поскольку образование СО2 является, по-видимому, основным процессом как при медленном окислении, так и при горении. Поэтому представляется насущным исследование этой проблемы, причем КИМ оказывается полезным при решении некоторых вопросов. [10]
Механизм этого окисления был разработан А. Н. Бахом еще в начале 1897 г. в его труде О роли перекисей в процессах медленного окисления. Энергия, необходимая для активации кислорода в процессе медленного окисления, не получается извне, а доставляется самим окисляемым веществом. Поэтому при обычных температурных условиях молекулярным кислородом могут окисляться лишь химически ненасыщенные, аутоксидабель-ные вещества, тогда как насыщенные остаются без изменения. Аутоксида-бельные вещества, приходя в соприкосновение с кислородом, не расщепляют его молекулу на свободные атомы ( как это думали раньше), а превращают эту молекулу в радикал, где только одна связь является разорванной. Указанный радикал и присоединяется к окисляемому веществу. При этом неизбежно должны образовываться перекиси, которые, являясь весьма неустойчивыми и химически активными веществами, способствуют дальнейшему окислению. [11]
Эта реакция является, по существу, полирекомбинацией: на стадии образования реакционных центров - радикалов - натрий играет роль перекиси, на стадии образования макромолекулы происходит рекомбинация радикалов, совершенно идентичная типичной полирекомбинации. [12]
Если подобный распад происходит и в условиях вулканизации, то роль диазоаминобензола как вулканизующего агента по нашему мнению аналогична разобранной выше роли перекиси бензоила. [13]
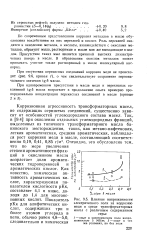 |
Влияние напряженности электрического поля на коррозию меди в среде трансформаторных масел с различным содержанием серы. [14] |
По современным представлениям коррозия металлов в масле обусловлена воздействием на них перекисей и кислот. Роль перекисей сводится к окислению металла, а кислоты, взаимодействуя с окислами металлов, образуют мыла, растворимые в масле или же выпадающие в осадок. Присутствие таких мыл является причиной высоких диэлектрических потерь в масле. В образовании окислов металлов может принимать участие также растворенный в масле молекулярный кислород. [15]
Страницы: 1 2