Рост - концентрация - компонент
Cтраница 1
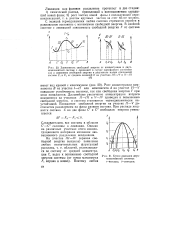
Рост концентрации компонента В на участке / - / / или компонента А на участке VI-V повышает устойчивость системы, так как свободная энергия F при этом понижается. Дальнейшее увеличение концентрации второго компонента на участках / / - / / / и V-IV приводит к повышению свободной энергии, и система становится термодинамически неустойчивой. Понижение свободной энергии на участке / / - V достигается разделением на фазы разного состава. [2]
В соответствии с этим правилом у смесей с максимальным давлением пара повышение давления вызывает рост концентрации компонента с большей теплотой парообразования, а у смесей с минимальным давлением пара - рост концентрации компонента с меньшей теплотой парообразования. [3]
В соответствии с этим правилом у смесей с максимальным давлением пара повышение давления вызывает рост концентрации компонента с большей теплотой парообразования, а у смесей с минимальным давлением пара - рост концентрации компонента с меньшей теплотой парообразования. [4]
Начиная от точки tA, температура плавления компонента А понижается по мере роста концентрации компонента В. Точно так же температура кристаллизации вещества В понижается с ростом концентрации примеси А. [5]
Начиная от точки tA, темпера тура плавления компонента А понижается по мере роста концентрации компонента В. Точно так же температура кристаллизации вещества В понижается с ростом концентрации примеси А. [6]
Однако обычно в системах с образованием малоустойчивых комплексных соединений уменьшению Д г с ростом концентрации к-того компонента предшествует некоторая область концентраций с увеличением Apt по мере возрастания концентрации к - того компонента. Это имеет место в системах, в которых комплексные анионы становятся преобладающими в растворе только при достаточно высоких концентрациях солей. [7]
На рис. 1.6 приведены три основных типа диаграмм фазового равновесия для систем, образующих непрерывный ряд твердых растворов. В диаграмме типа / отсутствуют экстрег аль-ные точки на линиях ликвидуса и солидуса; здесь с ростом концентрации компонента В температура начала кристаллизации непрерывно повышается. [8]
Как можно видеть из спектрограмм, но мере роста содержания хрома в образце возрастает относительная интенсивность длинноволновой, инфракрасной части спектра. Нередко в тех случаях, когда спектр люминесценции состоит из двух или более полос, отношение интенсивностей этих полос существенно изменяется с ростом концентрации люминесцирующего компонента в кристалле. При наличии такой зависимости количественные определения, в данном случае содержания хрома в рубине, могут быть сведены к измерению относительных интенсивностей свечения в различных участках спектра. Это измерение целесообразно производить объективным фотоэлектрическим методом, устанавливая перед окном фотоэлемента ( или фотоэлектронного умножителя) поочередно светофильтры, выделяющие необходимые участки спектра. Отношение показаний измерительного прибора при измерении через различные светофильтры может служить количественной мерой спектрального состава излучения, а следовательно, и искомой концентрации. [9]
 |
Значения мольных долей компонентов X., А /. при. [10] |
NH O нл - Это отвечает условиям существования так называемой кривой неполных экстремумов в тройных системах [4], которая начинается в точке XH. За пределами этой границы первый закон Коновалова не соблюдается. Это видно из рис. 1.3, где на левых восходящих ветвях давление в системе увеличивается с ростом концентрации труднолетучего компонента Н2О2 ( с ростом W) в полном противоречии с первым законом Коновалова. Такое свойство системы может представлять практический интерес. [11]
Состав азеотропа выражают в мольных или весовых процентах. При графическом изображении азеотропная точка бинарного или тройного азеотропа ( при данном давлении) точно соответствует экстремуму на кривой или поверхности давления пара. В 1910 г. русский ученый Вревский [15] сформулировал общее правило для изменения состава бинарного азеотропа с изменением давления. В соответствии с этим правилом, в случае максимума давления пара повышение давления вызывает рост концентрации компонента с большей теплотой парообразования, а у смесей с минимумом давления пара - рост концентрации компонента с меньшей теплотой парообразования. [12]
Состав азеотропа выражают в мольных или весовых процентах. При графическом изображении азеотропная точка бинарного или тройного азеотропа ( при данном давлении) точно соответствует экстремуму на кривой или поверхности давления пара. В 1910 г. русский ученый Вревский [15] сформулировал общее правило для изменения состава бинарного азеотропа с изменением давления. В соответствии с этим правилом, в случае максимума давления пара повышение давления вызывает рост концентрации компонента с большей теплотой парообразования, а у смесей с минимумом давления пара - рост концентрации компонента с меньшей теплотой парообразования. [13]
 |
Диаграммы равновесия. а - диаграмма у - х. 6 - треугольная диаграмма. [14] |
Каждой точке внутри треугольника соответствует тройная смесь, в к-рой концентрации компонентов А, В к С измеряются длинами перпендикуляров, опущенных на противолежащие стороны. В плоскости треугольника каждой темп-ре соответствует своя кривая растворимости - бинодальная кривая, отделяющая области гомогенных и гетерогенных р-ров. Точки на обеих ветвях последней, изображающие равновесные жидкие фазы, соединяются прямыми - конодами, напр. С имеет неодинаковую растворимость в А и В; поэтому критич. К не является экстремальной на бинодальной кривой. С ростом концентрации компонента С в тройной смеси составы равновесных жидких фаз постепенно сближаются вплоть до их совпадения в критпч. [15]
Страницы: 1