Рост - концентрация - соль
Cтраница 1
Рост концентрации солей в контактирующих растворах приводит к закономерному уменьшению набухаемости анионитов. Уменьшение в этом направлении различий в величинах объемов набухшей смолы отвечает наблюдаемому в подобных случаях снижению селективности анионитов. [1]
С ростом концентрации соли металла уменьшается эффективный объем гидратированного ( сольватированного) иона металла, разряжаемого на катоде. Это приводит к уменьшению эффективной энергии активации осаждения ( выделения) металла. Таким образом, энергия активации разряда ионов, обусловленная энергией дегидратации, соответственно больше в разбавленных растворах, нежели в концентрированных. [2]
По мере роста концентрации соли осаждаемого металла ( при сохранении других факторов - температуры, плотности тока - постоянными) скорость образования кристаллических зародышей уменьшается и покрытия становятся более грубозернистыми. [3]
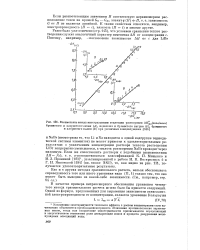 |
Взаимосвязь между интегральными теплотами растворения ДЯ288 ( квал / люль. [4] |
Увеличение акзотермичности теплового эффекта с ростом концентрации соли качественно объясняется преобладанием процесса сближения противоположно заряженных ионов, тогда как возрастание эндотермичности приписывается определяющей в энергетическом отношении роли дегидратации ионов и процесса разрушения молекулярных ассоциаций воды. [5]
Из таблицы 1 видно, что рост концентрации соли металла на 3 порядка ведет к росту предэкспонецциального множителя на 7 порядков. Иначе говоря, рост В обусловлен не столько ростом концентрации реагирующего вещества, сколько увеличением энтропии активации при электродных реакциях. [6]
Как видно из табл. 2 с ростом концентрации соли сернокислого родия в растворе скорость растворения снижается. Характер изменения скорости растворения в зависимости от концентрации электролита ( в пересчете на металлический родий) представлен на рисунке. [7]
Из рис. 2 видно, что с ростом концентрации соли поляризационные кривые сдвигаются в сторону менее положительных потенциалов. [9]
Из этой формулы следует, что с ростом концентрации соли рН начала образования гидроксида уменьшается, но всегда независимо от концентрации соли произведение концентраций ионов в степени их стехиометрических коэффициентов сохраняется постоянным. На значение произведения растворимости, выраженное в концентрациях, а не в основностях, влияет также ионная сила раствора. [10]
Величина т составляет несколько ангстрем и уменьшается с ростом концентрации соли. [11]
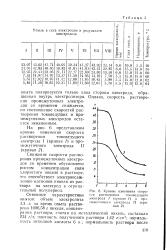 |
Кривые изменения скорости растворения токоведущего электрода / ( кривая / м промежуточного электрода II ( кри-пая 2. [12] |
Снижение скорости растворения промежуточных электродов со временем обусловлено ростом концентрации соли хлористого никеля в растворе, что способствует электроосаждению катионов никеля из раствора на электрод в отрицательный полупериод. [13]
Снижение теплоты испарения в водной области сначала увеличивается с ростом концентрации соли, поскольку здесь упорядочивание структуры вокруг иона не может перекрыть эффекта разрушения структуры воды. Затем это увеличение ослабевает и в области концентраций, близких к насыщению, теплота испарения из тройного раствора резко возрастает. По-видимому, молекулы компонентов растворителя входят здесь только в первую сольватную оболочку, связаны с ионами гораздо прочнее, чем молекулы воды и ацетонитрила в бинарном растворе. [14]
Было показано, что адсорбция сульфонатов нефти повышается с ростом концентрации соли [ 11, 17, 35 J. Найдено также, что адсорбция сульфонатов нефти сильно зависит от их эквивалентной массы. Адсорбцию последних эффективно понижает триполифосфат натрия. [15]
Страницы: 1 2 3 4 5
