Рост - поверхностная концентрация
Cтраница 1
Рост поверхностной концентрации приводит к повышению локальных концентраций хлорофилла в островках, сопровождаясь постепенным заполнением незанятой поверхности носителя. [1]
Рост поверхностной концентрации сопровождается возрастанием числа молекул, взаимодействующих между собой л-электронными облаками. Это выражается в повышении ДПС2, а также / Ci и К. [2]
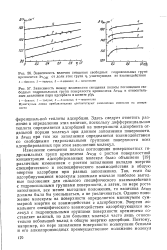
Как видно, во всех случаях с ростом поверхностной концентрации активного компонента каталитическая способность возрастает нелинейно, т.е. на неоднородной поверхности окиси алюминия имеется участки неодинаково пригодные для образования активных центров поликомпонентных катализаторов. Это открывает возможность оолее эффективно использовать активный компонент путем избирательного на несения его лишь на оптимальные для этого участка поверхности и получение сложных поликомпонентных катализаторов, например дегидрирования, путем нанесения в различной последовательности никеля на одну, наиболее благоприятную для этого металла группу участков, хрома - ка другую, платины - на третью и т.п. Полное использование поверхности носителя может создать условия для образования полифункциональных катализаторов и проведения слоимых стадийных процессов на одном катализаторе. Доказательством реальности этого направления могут служить полученные более эффективные крекирующие и дегидрирующие катализаторы с добавками окислов некоторых других металлов. [3]
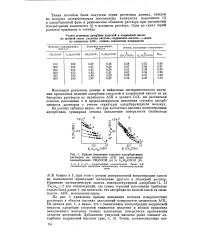 |
Кривые изменения составов адсорбционных растворов на силикагеле АСК при постоянных концентрациях СН3СООН ( а и CUH23COOH ( б. [4] |
АСК близка к 1, при этом с ростом поверхностной концентрации одного из компонентов происходит вытеснение другого в объемный раствор. Применяя математическую модель мономолекулярной адсорбции [4, 5] 2а / аю1 для концентраций, где сумма степеней заполнения приблизительно была равна 1, мы полагали, что адсорбция из данной смеси на силикагеле АСК мономолекулярна. [5]
Изменение смещения полосы поглощения поверхностных гидроксильных групп кремнезема AVOH с ростом поверхностной концентрации адсорбированных молекул было объяснено [19] различным изменением с ростом заполнения вкладов энергии специфического и неспецифического взаимодействия в общую энергию адсорбции при разных заполнениях. Так, если бы адсорбирующиеся молекулы занимали вначале наиболее выгодные положения для сильного специфического взаимодействия с гидроксильными группами поверхности, а затем, по мере роста заполнения, все менее выгодные положения, то величина AVOH должна была бы уменьшаться, а не увеличиваться. Однако положение молекулы на поверхности определяется минимумом суммарной энергии ее взаимодействия с адсорбентом. Энергия локального специфического взаимодействия адсорбирующихся молекул с гидроксильными группами поверхности кремнезема составляет важный, но для больших молекул часто лишь относительно небольшой вклад в общую энергию адсорбции. [7]
Этот вид изотермы, связанный с сильным уменьшением энергии адсорбции по мере роста поверхностной концентрации адсорбированного вещества, приводит к очень интересным кинетическим зависимостям, наблюдающимся на широком классе разнообразных объектов. [8]
 |
Изотермы адсорбции пара метанола па графитированной термической саже при разных температурах, полученные из хроматограмм ( 57. [9] |
Взаимодействие же ад-сорбат - адсорбат сильное и специфическое ( в этом случае возможна ассоциация молекул метанола в адсорбционном слое с образованием взаимных водородных связей; см. гл. По мере роста поверхностной концентрации молекул метанола между ними все сильнее проявляются специфические взаимодействия, и изотерма начинает круто подниматься. С дальнейшим увеличением давления пара начинает, однако, сказываться переход к адсорбции во втором и последующих слоях, что вызывает снова ускорение роста адсорбции, в результате чего изотерма адсорбции проходит вторую точку перегиба. [10]
 |
Выход по току при электро - 5. 00. [11] |
Выход по току натрия на свинцовом катоде определяется соотношением скоростей разряда ионов натрия из расплава хлорида натрия и растворения атомов натрия из свинцового катода в расплавленном электролите. Скорость растворения натрия возрастает с ростом поверхностной концентрации натрия в свинцовом катоде, а последняя в свою очередь, тем меньше, чем меньше толщина катода и чем интенсивнее его перемешивание. [12]
Это может быть следствием различий в закономерностях кристаллизации металла на данных носителях, обусловленных, например, неодинаковой прочностью связи металл - носитель и связанной с этим разной его поверхностной подвижностью. Наиболее резкое уменьшение дисперсности с ростом поверхностной концентрации палладия наблюдается для SiO2, наименее резкое - - для А12О3 и AISi; на угле в исследованном интервале изменения концентрации дисперсность Pd вообще не изменяется. На А12О3, AISi, угле дисперсность Pd наиболее высока. Низкая дисперсность достигается при нанесении Pd на цеолит или же на носители с малой поверхностью - корунд, карборунд. [13]
Для калиевых пленок Ет уменьшалась с ростом поверхностной концентрации от 16 ккал / г-атом при очень малых заполнениях до 6 7 ккал / г-атом при поверхностной концентрации 4 8 - 10й атом / см2; такое падение Ет в этом случае было объяснено наличием способствующих растеканию сил, обусловленных взаимным отталкиванием адсорбированных ионов. [14]
Для таких ингибиторов коррозии стали, как производные анилина в работе [35] показано, что переход от электрофильных к нук-леофильным заместителям приводит к усилению рекомбинационно-го и ослаблению разрядного торможения при выделении водорода. Это возникает вследствие усиленной хемосорбции молекул ( с высокой плотностью электронов на центральном атоме азота) на каталитически активных центрах поверхности железа. Блокирование таких определяющих рекомбинацию водородных атомов центров обусловливает рост поверхностной концентрации атомов водорода и усиление его внедрения в железо. [15]
Страницы: 1 2