Рост - коэффициент - распределение
Cтраница 2
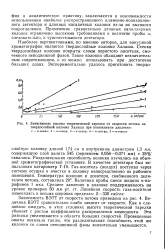 |
Зависимость высоты теоретической тарелки от скорости потока на твердослойной колонке Халаша при пониженном давлении. [16] |
Величина ВЭТТ сравнительно слабо зависит от скорости. Как и следовало ожидать, в этих условиях высота теоретической тарелки убывает с ростом коэффициента распределения компонента. Эта разница увеличивается в области больших скоростей. Проведенные опыты показали также, что разделительная способность этой же колонки со слоем неподвижной фазы значительно уменьшается. [17]
 |
Зависимость коэффициента сопротивления массопередаче в жидкости с-к от коэффициента емкости колонки k. [18] |
Эффективность колонки определяется не только свойствами неподвижной фазы, но и межмолекулярным взаимодействием сорбата с неподвижной фазой. Наиболее заметные колебания сопротивления массопередаче приходятся на значения коэффициентов емкости до 20; при более высоких значениях этого параметра сопротивление массопередаче снижается незначительно с ростом коэффициента распределения. Отсюда вытекает одно из основных требований к неподвижной фазе для обеспечения эффективного разделения смесей: коэффициенты емкости трудноразделяемых веществ должны быть выше 20 и, следовательно, неподвижная фаза должна достаточно хорошо растворять компоненты смеси. Это требование необходимо учитывать наряду с избирательностью неподвижной фазы, ибо избирательность не связана с абсолютным значением коэффициента распределения. [19]
Высокая селективность некоторых неорганических ионообменников была использована в хроматографии с применением бумаги, пропитанной соответствующими веществами [21] ( см. также стр. В табл. 21 показано, что коэффициенты распределения ионов цезия и таллия из 0 1 М раствора NH4NO3 при рН 2 имеют высокие значения. Принимая во внимание тенденцию роста коэффициентов распределения в ряду щелочных металлов, можно предполагать, что и для франция величина этого коэффициента должна быть очень высокой. [20]
Высокая селективность некоторых неорганических ионообменников была использована в хроматографии с применением бумаги, пропитанной соответствующими веществами [21] ( см. также стр. В табл. 21 показано, что коэффициенты распределения ионов цезия и таллия из 0 1 М раствора NH4NOs при рН 2 имеют высокие значения. Принимая во внимание тенденцию роста коэффициентов распределения в ряду щелочных металлов, можно предполагать, что и для франция величина этого коэффициента должна быть очень высокой. [21]
Присутствие солей вызывает несколько эффектов. Поскольку речь идет о солях с одноименным ионом, введение их означает увеличение концентрации галогенид-ионов ( при той же концентрации ионов водорода), а это способствует образованию галогенидных комплексов с большим числом лигандов. Если металл извлекается в виде высшего комплекса, добавление солей почти наверняка приведет к росту коэффициентов распределения; если экстрагирующийся комплекс - промежуточный, результат может быть и иной. Введение соли в дополнение к уже имеющейся в системе галогеноводородной кислоте вызывает понижение активности воды в водной фазе, что также благоприятствует экстракции. [22]
Высокие значения коэффициентов распределения при извлечении аминами с угловым азотом указывают на высокую прочность сольватов ( это хорошо согласуется с данными о том, что энергия водородной связи в системе пиридин - вода близка к соответствующему значению для системы вода - вода [44]), на близость значений параметров Гильдебранда для сольвата и экстрагента, а также на невысокие значения константы диссоциации в фазе органического растворителя. На последнее предположение указывает тот факт, что адсорбция перренат-иона на анионитах из фазы экстракта незначительна. Однако при разбавлении пиридинового экстракта водой резко-возрастает значение диэлектрической проницаемости, что приводит к повышению константы диссоциации сольвата, и естественно, к росту коэффициента распределения. [23]
Высокие значения коэффициентов распределения при извлечении аминами с угловым азотом указывают на высокую прочность сольватов ( это хорошо согласуется с данными о том, что энергия водородной связи в системе пиридин - вода близка к соответствующему значению для системы вода - вода [44]), на близость значений параметров Гильдебранда для сольвата и экстрагента, а также на невысокие значения константы диссоциации в фазе органического растворителя. На последнее предположение указывает тот факт, что адсорбция перренат-иона на анионитах из фазы экстракта незначительна. Однако при разбавлении пиридинового экстракта водой резко возрастает значение диэлектрической проницаемости, что приводит к повышению константы диссоциации сольвата, и естественно, к росту коэффициента распределения. [24]
Закономерности влияния разбавителей на экстракцию солями ЧАО, по-видимому, во многих случаях отличаются от соответствующих закономерностей, наблюдаемых при экстракции солями аминов. Это, вероятно, объясняется более высокой полярностью и заметной ассоциацией молекул солей ЧАО. Например [534], коэффициенты распределения Pt ( IV) при экстракции хлоридом ЧАО с использованием в качестве разбавителей спиртов или жирных кислот, сольватирующих анионы солей ЧАО, снижаются по сравнению с несольватирующим неполярным керосином. Однако применение дихлорэтана и хлороформа, несмотря на их некоторую способность сольватировать анионы соли ЧАО, приводит к росту коэффициентов распределения. Последнее, по-видимому, связано с деполимеризацией и увеличением экстракционной способности солей ЧАО и их совместимости с разбавителем при добавлении этих относительно полярных разбавителей. [25]
Коэффициент распределения элемента остается постоянным при изменении концентрации, если состав соединений в органической и водной фазах при этом не меняется. Однако в ряде случаев соединения элемента полимеризуются ( или вступают в состав ионных ассоциатов) или, наоборот, диссоциируют в одной из фаз, причем степень протекания этих процессов зависит от концентрации элемента. При этом коэффициенты распределения изменяются с концентрацией. В общем, полимеризация ( ионная ассоциация) в органической фазе приводит к уменьшению коэффициентов распределения с уменьшением концентрации элемента, полимеризация же в водной фазе и диссоциация в органической ведут к росту коэффициентов распределения при переходе к меньшим концентрациям. [26]
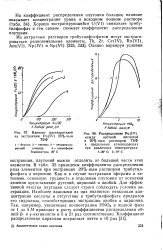 |
Влияние растворителей.| Распределение Pu ( IV между азотной кислотой и 20 % - ным раствором ТБФ в предельных углеводородах при различных температурах. / - 20 С. 2 - 70 С. [27] |
В табл. 35 приведены коэффициенты распределения ряда элементов при экстракции 20 % - ным раствором трибутил-фосфата в керосине. Как и в случае экстракции эфирами и ке-тонами, основную трудность в отделении плутония от осколков деления представляют рутений, цирконий и ниобий. Для эффективной очистки плутония следует строго соблюдать условия экстракции. Наиболее важными из них являются: невысокая концентрация кислоты и отсутствие в трибутилфосфате продуктов его гидролиза, способствующих экстракции ниобия и циркония. Так, например, увеличение концентрации HNO3 в водной фаза от 1 до 5 М приводит к росту коэффициентов распределения общей Р - и у-активности в 5 и 21 раз соответственно. [28]
Страницы: 1 2