Рост - скорость - окисление
Cтраница 1
Рост скорости окисления при малых концентрациях титана связан с растворением титана в NiO. В состав окалины кроме NiO, NiCr2O4 и Сг2О3 входят NiTiO3 и рутил, причем концентрация последних с течением времени возрастает. [1]
С ростом скорости окисления тетралина в основные продукты реакции должна увеличиваться и скорость образования побочных продуктов, среди которых, как было показано ранее [3], присутствует такой известный ингибитор жидкофазпых реакций окисления, как нафтол-1. [2]
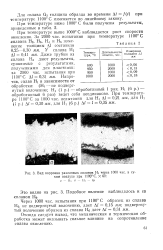 |
Вид коррозии различных сплавов HI через 1000 час. в сухом воздухе при 1100 С. X 60. [3] |
При температуре выше 1000 С наблюдается рост скорости окисления. [4]
Однако в концентрированной соляной кислоте наблюдается рост скорости окисления по мере увеличения ее концентрации. [5]
По наблюдениям Баура, Бриджеса и Фассела, в интервале линейного окисления давление при 600 - 700 С не оказывало никакого влияния на процесс окисления; при 750 - 850 С это влияние было незначительно и сводилось при изменении давления от 1 до 35 атм к двукратному росту скорости окисления. [6]
Окисление сернистых компонентов в составе гудрона западно-сибирской нефти уке в начальном периоде идет с высокой скоростью окисления ( рис. 2 6), которая затем заметно снижается в случае окисления диалкилсульфидов. Причем момент снижения скорости окисления диалкилсульфидов по времени совпадает с ростом скорости окисления ароматических углеводородов в этом же сырье. Скорость окисления алкилдййрилсульфидов в ходе всего процесса практически не меняется и только в конечной стадии несколько растет. Полученные экспериментальные результаты позволяют обосновать существование ингибированного режима окисления ароматических углеводородов в составе сернистого сырья. [7]
При окислении образцов, не отожженных после алитирования, на поверхности образовывалась пленка А12О3, существенно замедляющая испарение алюминия. Покрытие хорошо защищает металл от окисления при температуре выше 1100 С и давлении кислорода 0 1 мм рт. ст. Увеличение давления кислорода во всех случаях приводит к росту скорости окисления. [8]
Скорость образования спиртов в некатализированном - окислении н с добавкой стеарата марганца до накопления их 12 - 13 % вес. Аналогичное явление имеет место и для смешанного Мп - К катализатора. С повышением концентрации спиртов выше 12 % скорость окисления их растет. Рост скорости окисления спиртов при достижении их концентрации свыше 12 % обусловлен тем, что С - Н - связь спиртовой группы гораздо слабее С - Н связи углеводорода. Поэтому, чем выше концентрация спирта, тем быстрее он окисляется, и в связи с этим растет общая скорость окисления, что и отмечалось нами выше. [9]
Для медноникелевых сплавов с содержанием до 25 % Си Пиллинг и Бедуорт фактически получили не постоянную скорость окисления, а несколько возрастающую с ростом содержания меди. Так, Вагнер предполагает, что рост скорости окисления может быть обусловлен зарождением в начале процесса центров кристаллизации обоих окислов и что вследствие большей подвижности катионов в закиси меди СигО по сравнению с окисью никеля NiO неустойчивая закись меди способна некоторое время расти одновременно с окисью никеля. [10]
Процесс обезуглероживания углеродистых сталей приводит к уменьшению скорости их окисления в воздухе. Скорость окисления сталей понижается с увеличением содержания в них углерода и тем сильнее, чем выше температура. При низких температурах ( 850 С) эффект обезуглероживания снижается и уменьшается его влияние на жаростойкость, а изотермы жаростойкости имеют два участка, соответствующих доэвтектоидным и заэвтектоидным сталям. На каждом из них жаростойкость повышается с увеличением содержания в стали углерода, но переход от доэвтектоидных сталей к заэвтектоидным сопровождается ростом скорости окисления, что указывает на различную скорость окисления углерода вторичного цементита и перлита. [11]
До превращения 25 % углеводорода в некатализированжш окислении скорость окисления растет с 1 25 % до 2 0 % вес. Скорость накопления спиртов до превращения 24 % углеводовода постоянна и составляет 0 65 % вес. После накопления 12 % спиртов скорость окисления их растет, а скорость образования снижается. При достижении концентрации 15 % устанавливается кинетически равновесное состояние, при котором скорость образования спиртов равна скорости их расходования. Такое отношение скоростей наступает после превращения 50 % углеводорода, когда скорость - окисления начинает зависеть от концентрации углеводорода. Нетрудно заметить, что рост, скорости окисления наступает с момента роста скорости окисления спиртов, то-есть, когда в разветвлении цепи принимают участие спирты. Скорость образования свободных и связанных кислот растет до 1 25 % вес. Рост скорости образования ( кислот совпадает с ростом скорости окисления углеводорода, в том числе скорости окисления спиртов. [12]
До превращения 25 % углеводорода в некатализированжш окислении скорость окисления растет с 1 25 % до 2 0 % вес. Скорость накопления спиртов до превращения 24 % углеводовода постоянна и составляет 0 65 % вес. После накопления 12 % спиртов скорость окисления их растет, а скорость образования снижается. При достижении концентрации 15 % устанавливается кинетически равновесное состояние, при котором скорость образования спиртов равна скорости их расходования. Такое отношение скоростей наступает после превращения 50 % углеводорода, когда скорость - окисления начинает зависеть от концентрации углеводорода. Нетрудно заметить, что рост, скорости окисления наступает с момента роста скорости окисления спиртов, то-есть, когда в разветвлении цепи принимают участие спирты. Скорость образования свободных и связанных кислот растет до 1 25 % вес. Рост скорости образования ( кислот совпадает с ростом скорости окисления углеводорода, в том числе скорости окисления спиртов. [13]
Страницы: 1