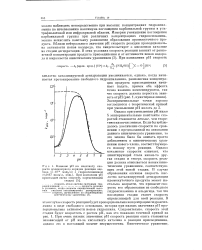
Нейтральное значение
Cтраница 4
Выше 45 - 50 С вследствие тепловой денатурации происходит потеря стабильности белковых молекул ( из-за потери гидратной оболочки), что сопровождается резким снижением растворимости белков в области нейтральных значений рН, и таким образом происходит термоосаждение белков. [46]
В щелочной среде более интенсивно протекают реакции образования мыл высших карбоновых кислот и их предпочтительная адсорбция на границе раздела фаз с образованием более прочного слоя, чем при кислых и нейтральных значениях рН водной фазы. С солями двухвалентных металлов при повышений значений рН наблюдается также образование гидроксидов коллоидной степени дисперсности. [47]
При подаче кислых сточных вод рН на выходе аппарата возрастает и стремится к нейтральному значению, а в случаи щелочных растворов рН на выходе снижается и также стремится к нейтральному значению. Никаких специальных реагентов при этом не требуется. [48]
В щелочной среде более интенсивно протекают реакции образования металлических мыл высших карбоновых кислот и их предпочтительная адсорбция на границе раздела фаз с образованием более прочного слоя, чем при кислых и нейтральных значениях рН водной фазы. С солями двухвалентных металлов при повышении значений рН наблюдается также образование гидрооксидов коллоидной степени дисперсности. [49]
Легкость образования этих заряженных соединений намного перекрывает низкую электроотрипательность азота, и поэтому азот действует как ловушка электронов более эффективно, чем кислород, который хотя и более электроотрицателен, но образует при нейтральных значениях рН катион настолько трудно, что в таком механизме реакции он фактически неактивен как акцептор электрона. Наоборот, легкость, с которой азот может отдавать электронную пару, позволяет ему действовать как своего рода малоактивный карбанион; енамин легко может отдавать электроны с образованием новой связи к углеродному атому ( XL), в то время как образование истинного карбаниона ( XLI) - это процесс, характеризующийся значительно более высокой энергией. [50]
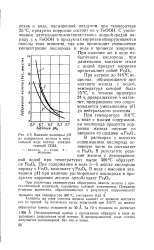 |
Влияние величины рН на содержание железа в питательной воде котлов электростанций США. [51] |
При нагреве до 316 С вещества, образующиеся при контакте железа с водой, температура которой была 25 С, в течение примерно 24 ч, превращаются в магнетит; превращение это сопровождается уменьшением рН до нейтрального значения. [52]
Химическая очистка емкостей и трубопроводов из углеродистой стали включает в себя: 1) очистку и обезжиривание прокачиванием 8 - 10-процентного раствора каустической соды при температуре около 65 С; 2) промывку чистой водой; 3) очистку от песка, ржавчины и окалины прокачиванием 10-процентного раствора соляной кислоты с добавкой 0 25 - 0 50 % бифтористого аммиака; раствор, нагретый не менее чем на 65 С, должен циркулировать в трубопроводе 4 ч или более в зависимости от его состояния; 4) просушку трубопровода сухим азотом; 5) промывку его чистой водой до получения нейтрального значения показателя концентрации водородных ионов рН; 6) нейтрализацию трубопровода 0 25-процентным раствором лимонной кислоты. Операция нейтрализации может быть заменена просушкой трубопровода горячим воздухом, наполнением его смазочным маслом и последующей продувкой горячим воздухом. [53]
Измеряя уменьшение поглощения карбонильной группы при различных койцентрациях гидроксиламина, можно вычислить константу равновесия образования промежуточного продукта. Вблизи нейтрального значения рН скорость реакции пропорциональна активности ионов водорода, что свидетельствует о кислотном катализе на стадии дегидратации. [55]
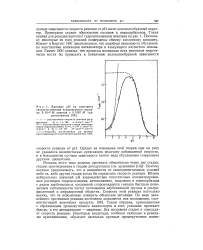 |
Влияние рН на константу скорости реакции псевдопервого порядка 5 - 10 - 4УИ ацетона с 0 0167 М гид-роксиламина [ 98 J. [56] |
Поэтому логично предположить, что в зависимости от экспериментальных условий либо та, либо другая стадия могла бы определять скорость реакции. Вблизи нейтральных значений рН взаимодействие относительно концентрированных растворов гидроксиламина, метоксиамина, гидразина и семикарбазида с рядом карбонильных соединений сопровождается сначала быстрым понижением интенсивности частот поглощения карбонильной группы в ультрафиолетовой и инфракрасной областях. Скорость этой реакции настолько велика, что ее невозможно измерить обычными методами. Таким образом, присоединение с образованием промежуточного аминоспирта в этих условиях протекает быстро, а его дегидратация - медленно. Эта последняя стадия и определяет скорость реакции. [57]
Карбоксильные ионофоры могут входить в литшдные фазы либо как электронейтральные цвиттер-ионные комплексы, либо как незаряженная недиссоциярованная карболовая - кислота. При нейтральных значениях рН только небольшое количество ионофора проходит липидный барьер в виде заряженных частиц; следовательно, этот класс ионофоров фактически не проявляет себя электрически по отношению к мембранам. При более высоких значениях рН несвязанная в комплекс карбоксилатная форма этих ионофоров, по-видимому, становится достаточно преобладающей, чтобы проводить ток и вызывать электрометрически детектируемые эффекты на мембранах. [58]
Страницы: 1 2 3 4