Рудингер
Cтраница 1
Рудингер в i963 г. В статье Органическая химия в оинтезе пептидов он показал, что в химии пептидов широко используются методы синтетической органической химии, однако выбор этих методов должен ооответствсвать требованиям к синтезу биополимеров, какими являются полипептиды. [1]
Рудингер и Шорм [1861] получили глутатион принципиально тем же самым путем. Различие заключалось лишь в синтезе H-Cys ( Bzl) - Gly-OEt, который был проведен реакцией между S-бензилцистеином и этиловым эфиром глицина в тетрагидро-фуране с использованием N-карбоксиангидридного метода. [2]
Рудингера [2.47] были определены значения коэффициента сопротивления стеклянных шариков в потоке газа при прохождении слабых ударных волн. [3]
В последние годы Рудингером [1850] начаты исследования по синтезу циркулина А. Для этой цели был получен модельный пептид, схема синтеза которого приведена на рис. 119; более подробные данные пока не опубликованы. [4]
По методу Хонцля и Рудингера [233] можно проводить азидную конденсацию прямо в органическом растворителе, используя для этого трет-бутилнитрит. Гидразинолиз эфирных групп более длинных N-защищенных пептидов часто бывает трудным. Можно использовать N-замещенные гидразиды ( разд. Соответствующий пептидный фрагмент, полученный по одному из известных методов синтеза, вводят в азидную конденсацию после селективного удаления защитной группы гидразида. Поскольку азиды ациламинокислот легко рацемизуются при катализе основаниями [235], при азидных конденсациях следует избегать контакта с основаниями. Для нейтрализации солей аминокомпонентов вместо триэтиламина целесообразно применять N N - flHH3onpom i3THnaMHH и N-алкилморфолин. [5]
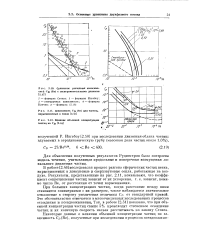 |
Сравнение расчетных зависимо-стей Од ( Re с экспериментальными данными.| Зависимость Сд ( Re для частиц, / ff впрыскиваемых в сопло [ t ].| Влияние объемной концентрации частиц на Сд. [6] |
Для объяснения полученных результатов Рудингером была построена модель течения, учитывающая продольные и поперечные возмущения локального движения частиц. [7]
 |
Синтез N-Me Туг2 - окситоцина ( температуры плавления исправлены ( Хегенин и Буассона. [8] |
Биологическая активность свободного нонапептида, определенная Рудингером [1851], совпадает с приведенными выше результатами швейцарских исследователей. [9]
НВг в уксусной кислоте изучали Блага и Рудингер [557], кроме того, Лоссе и др. [558] проводили кинетические исследования кислотности деблокирования N - и С-защитных групп. [10]
Другой, часто встречающейся побочной реакцией при азид-ном синтезе является образование амидов. По мнению Хонцля и Рудингера [1058], образование амида не связано с перегруппировкой азида, а является следствием побочной реакции гидразида с азотистой кислотой. Это подтверждается тем фактом, что при синтезе азидов взаимодействием соответствующих хлорангидридов с азидом натрия образования амидов никогда не наблюдалось. [11]
Интересные результаты получены при замене изолейцинового остатка в положении 3, играющего существенную роль в проявлении биологической активности, на остатки других аминокислот. Активность соответствующих аналогов убывает в следующем порядке: IleuValLeuPheTyrTry. Рудингер и Крейчи [1856] исследовали зависимость между вводимой дозой и последующим эффектом на примере alleu3 -, NVal3 -, Val3 -, NLeu3 - и Ьеи3 - окситоцинов. Авторам удалось показать, что уменьшение активности аналогов, замещенных в положении 3, объясняется снижением эффективности связывания с рецептором. Окситоцин ( XX) [167, 297, 1855, 1856] при испытаниях in vitro на матке крысы и на кровяное давление у птиц в восемь раз менее активен, чем окситоцин. Таким образом, для Уа13 - окситоцина наблюдается более избирательная окситотическая активность, чем для окситоцина, что проявляется более четко в опытах in vivo, чем in vitro. Интересно, что замена изолейцинового остатка на какую-либо другую ароматическую аминокислоту ( Туг3 - оксито-цин XIX [166, 288] и Тгу3 - окситоцин XVIII [166, 896]) приводит к практически неактивным соединениям. [12]
 |
Предположительная биологически активная конформация окситоцина. [13] |
Проверенная концепция была перенесена также на синтез вазопрессина и хорошо зарекомендовала себя при получении аналогов с различными фармакологическими свойствами. Особый интерес представляют аналоги с продолжительным раздельным действием на молочные железы или матку. Так, например, [ 2 - О-метилтирозин ] окситоцин проявляет специфическое действие на матку in situ ( Рудингер, 1967 г.), в то время как дезамино - [ 4-глутамил - 7-метиловый эфир, карбо ] окситоцин ( Йошт и др.) действует преимущественно на молочные железы. Большой интерес вызывал синтезированный Маннингом [623] [ ТЬг4 ] окситоцин, оказывающий более специфическое и более сильное действие, чем природный гормон. Повышенный биологический эффект в результате обычной замены аминокислоты без дальнейших структурных модификаций, как было сделано у многих активных аналогов, объясняется отличным от имеющего место в случае природного окситоцина и еще не полностью интерпретируемым механизмом гормон-рецепторного взаимодействия. Этот феномен был назван химической мутацией. [14]
Де-сульфурирование окситоцина, его восстановление или восстановление с последующим алкилированием приводят к биологически неактивным соединениям. В течение длительного времени не было получено каких-либо дополнительных данных о роли дисульфидной связи в проявлении окситоцином биологической активности. Недавно Рудингер и Йошт [ 1855а ] заменили с этой целью один атом серы на метиленовую группу. Лактам Туг-Ileu - Glu ( NH2) - Asp ( NH2) - S - ( 3-карбоксипропил) - Cys-Pro-Leu-Gly - ЫН2 ( дезамино-карба 1-окситоцин) был получен в результате восстановления Cbo-Tyr-Ileu-Glu ( NH2) - Asp ( NH2) - Cys ( Bzl) - Pro-Leu-Gly - NH2 натрием в жидком аммиаке, алкилирования in situ грег-бутиловым эфиром 4-иодмасляной кислоты, удаления трет-бутильной группы трифторуксусной кислотой и наконец заключительной циклизации в присутствии N-этил-б - фенилизоксазо-лий - З - сульфоната. [15]
Страницы: 1