Отрицательное значение - реакция
Cтраница 1
Отрицательное значение реакции S9 говорит о том, что в действительности эта реакция направлена в сторону, противоположную принятой, i; к у. А и стержень 9 сжат. Аналогично могут быть определены методом сечений усилия в любых стержнях этой фермы. [1]
Отрицательное значение реакции 6 показывает, что в действительности она направлена в противоположную сторону и стержень / не растянут, как мы предполагали, а сжат. [2]
Отрицательное значение реакций NI указывает, что устойчивость крана не обеспечивается, и левые колеса при таком приложении сил оторвутся от опорного круга. Для обеспечения устойчивости крана следует включить в работу центральную цапфу. Тогда равнодействующая 2JV может быть уравновешена реакциями N2 и усилием Nc цапфы. [3]
Отрицательное значение реакции Si показывает, что в действа тельности она направлена в противоположную сторону и стерженб 1 не растянут, как мы предполагали, а сжат. [4]
Отрицательное значение реакции RA означает, что она направлена вниз, а не вверх, как показано на рис. 106, б, потому что момент силы F относительно опоры В больше, чем момент равномерно распределенной нагрузки. [5]
Отрицательное значение реакции RA означает, что она направлена вниз, а не вверх, как показано на рис. 104, б, потому что момент силы Р относительно опоры В больше, чем момент равномерно распределенной нагрузки. [6]
Почему во многих случаях при отрицательных значениях АС реакции практически не протекают. [7]
Из какого уравнения следует, что при отрицательных значениях ДО реакции константа равновесия должна быть больше единицы. [8]
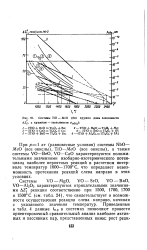 |
Системы TiO - МеО ( без кружка даны зависимости. [9] |
Системы VO - MgO, VO - SrO, VO - BaO, VO - А12Оз характеризуются отрицательными значениями AZ реакции соответственно при 1500, 1700, 1700 и 1500 С ( см. табл. 24), что свидетельствует о возможности осуществления реакции слева направо, начиная с указанного значения температур. [10]
К этой группе следует отнести CaO, ( 3 - C2S, C3S, C2A, СА, CaSO4 0 5Н2О, MgO. Здесь, наоборот, отрицательное значение AZ реакций достаточно велико, а изменение координации ионов Са в нормальных условиях затруднено, поэтому и здесь для проявления вяжущих свойств нужны специальные условия в виде гидротермальной обработки. [11]
Для экономичного и рационального использования этого вида сырья полезно проанализировать все возможные реакции превращения метана в устойчивые продукты. Для этой цели нужно записать все мыслимые реакции и составить для них таблицу изменений энергии Гиббса при нескольких температурах. В табл. VII.9 приведены результаты термодинамического анализа некоторых реакций превращения метана в другие соединения при давлении 1 атм. Изменения энергии Гиббса указанных реакций рассчитаны при 400, 600, 800 и 1000 К. Следует отметить, что в табл. VII.9 рассмотрены только такие реакции, данные для всех участников которых приведены в настоящей книге, причем перечень реакций ни в коей мере не является исчерпывающим. Тем не менее даже в этом случае информация о реакционной способности метана очень полезна и позволяет оценить возможности получения из него различных ценных продуктов. Рассмотрим подробнее некоторые реакции, представляющие особый интерес. Отрицательные значения AGr реакций 6а, 7а, 8а и 9а свидетельствуют о самопроизвольном протекании замещения атомов водорода в метане на атомы хлора; однако из величин AGr реакций 66, 76, 86 и 96 видно, что с увеличением числа атомов водорода, замещенных хлором, этот процесс постепенно становится все менее благоприятным. Величины AGr реакций 11 и 37 свидетельствуют о возможности использования метана в качестве исходного сырья для синтеза углеводородов. Отрицательные значения ДО0 реакций 14, 18 и 43 указывают на возможность образования Н202 в процессе окисления метана. Термодинамические параметры реакции 23 подчеркивают трудность осуществления синтеза уксусной кислоты из двуокиси углерода и метана и свидетельствуют о легкости протекания обратной реакции. [12]
Для экономичного и рационального использования этого вида сырья полезно проанализировать все возможные реакции превращения метана в устойчивые продукты. Для этой цели нужно записать все мыслимые реакции и составить для них таблицу изменений энергии Гиббса при нескольких температурах. В табл. VII.9 приведены результаты термодинамического анализа некоторых реакций превращения метана в другие соединения при давлении 1 атм. Изменения энергии Гиббса указанных реакций рассчитаны при 400, 600, 800 и 1000 К. Следует отметить, что в табл. VII.9 рассмотрены только такие реакции, данные для всех участников которых приведены в настоящей книге, причем перечень реакций ни в коей мере не является исчерпывающим. Тем не менее даже в этом случае информация о реакционной способности метана очень полезна и позволяет оценить возможности получения из него различных ценных продуктов. Рассмотрим подробнее некоторые реакции, представляющие особый интерес. Отрицательные значения AGr реакций 6а, 7а, 8а и 9а свидетельствуют о самопроизвольном протекании замещения атомов водорода в метане на атомы хлора; однако из величин AGr реакций 66, 76, 86 и 96 видно, что с увеличением числа атомов водорода, замещенных хлором, этот процесс постепенно становится все менее благоприятным. Величины AGr реакций 11 и 37 свидетельствуют о возможности использования метана в качестве исходного сырья для синтеза углеводородов. Отрицательные значения AGr реакций 14, 18 и 43 указывают на возможность образования Н202 в процессе окисления метана. Термодинамические параметры реакции 23 подчеркивают трудность осуществления синтеза уксусной кислоты из двуокиси углерода и метана и свидетельствуют о легкости протекания обратной реакции. [13]
Для экономичного и рационального использования этого вида сырья полезно проанализировать все возможные реакции превращения метана в устойчивые продукты. Для этой цели нужно записать все мыслимые реакции и составить для них таблицу изменений энергии Гиббса при нескольких температурах. В табл. VII.9 приведены результаты термодинамического анализа некоторых реакций превращения метана в другие соединения при давлении 1 атм. Изменения энергии Гиббса указанных реакций рассчитаны при 400, 600, 800 и 1000 К. Следует отметить, что в табл. VII.9 рассмотрены только такие реакции, данные для всех участников которых приведены в настоящей книге, причем перечень реакций ни в коей мере не является исчерпывающим. Тем не менее даже в этом случае информация о реакционной способности метана очень полезна и позволяет оценить возможности получения из него различных ценных продуктов. Рассмотрим подробнее некоторые реакции, представляющие особый интерес. Отрицательные значения AGr реакций 6а, 7а, 8а и 9а свидетельствуют о самопроизвольном протекании замещения атомов водорода в метане на атомы хлора; однако из величин AGr реакций 66, 76, 86 и 96 видно, что с увеличением числа атомов водорода, замещенных хлором, этот процесс постепенно становится все менее благоприятным. Величины AGr реакций 11 и 37 свидетельствуют о возможности использования метана в качестве исходного сырья для синтеза углеводородов. Отрицательные значения AGr реакций 14, 18 и 43 указывают на возможность образования Н202 в процессе окисления метана. Термодинамические параметры реакции 23 подчеркивают трудность осуществления синтеза уксусной кислоты из двуокиси углерода и метана и свидетельствуют о легкости протекания обратной реакции. [14]
Страницы: 1