Свертывание - молекула
Cтраница 1
Свертывание молекул в клубки, о чем было сказано ранее, и увеличение расстояния между основными цепями повышает способность привитых сополимеров к деформациям, что и проявляется в увеличении разрывного удлинения. [2]
При удлинении цепи свертывание молекулы в клубок уменьшает ее сопротивление течению, вследствие чего зависимость вязкости от молекулярного веса отклоняется от прямой пропорциональности. [3]
Для того чтобы проявилось свертывание молекул в клубки, поперечные сшивки должны быть наведены в состоянии предварительного продольного натяжения трехмерной молекулярной сетки полимерного образца. [4]
Точное знание конфигурации молекулы фермента, включая конформацию протеина в складках или при свертывании молекул в спираль, а также химической структуры вблизи активного центра может оказаться весьма важным. Так, например, активность фермента может быть нарушена при нагревании или воздействии химических реагентов ( кислот, оснований или концентрированных растворов солей), изменяющих конформацию протеина путем денатурации. Кроме того, активность может быть потеряна в результате действия ингибиторов. Последние обычно действуют при взаимодействии с активными центрами и используются для определения числа активных центров в отдельной молекуле фермента, а также для получения данных об их химическом строении. [5]
В то же время на цепные молекулы высокомолекулярных соединений оказывает также влияние энергия межмолекулярного взаимодействия, препятствующая протеканию описанных выше явлений свертывания молекул полимера в статистические клубки. [6]
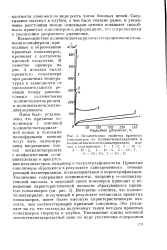
Тенденция к свертыванию макромолекул в клубки возрастает с повышением концентрации ксантогената. Свертывание молекул в клубки начинается 45 при концентрации 0 2 %, и далее оно возрастает с повышением концентрации ксантогената в растворе. Что касается влияния концентрации едкого натра, то было установлено, что с ее повышением степень свертывания макромолекул в клубки возрастает. [7]
Помимо изгибов, определяющих вторичную структуру, в полипептидных цепях белка, как правило, имеются изгибы, обусловленные внутримолекулярными силами, характер которых не является ни регулярным, ни периодическим; это так называемая третичная структура молекулы, определяющая тип свертывания цепи данного белка в целом. Благодаря такому свертыванию молекулы многих глобулярных белков, например гемоглобина, хотя и состоят из длинных полипептидных цепей, тем не менее имеют почти сферическую форму. В большинстве случаев свертывание происходит в результате взаимодействия боковых групп белка, однако его причиной могут быть также и взаимодействия групп, составляющих остов полипептидной цепи. [8]
 |
Строение молекулы политетрафторэтилена. спирализация полиэтиленовой цепи ( ср. 22. [9] |
Принципиально новый случай имеет место, если в цепь нерегулярно включаются звенья иного типа, изменяющие ее хребет, или же к регулярной цепи из одинаковых звеньев нерегулярно прикрепляются крупные радикалы, создающие пространственные затруднения и нарушающие поэтому геометрическую однообразность хребта. Это приводит к свертыванию молекулы самым произвольным образом, так как никаких условий для выдерживания периодичности в некотором направлении не остается. Свертыванию содействует и сопутствует образование тех или иных перекрестных связей между участками свернутой цепи. Свернутые цепные молекулы уже являются в сущности глобулярными. Здесь нужно различать два случая. Если нерегулярность является статистической, неравномерной, то каждая молекула такого полимера будет свернута на свой манер и все эти глобулярные, клубковые молекулы будут непохожи друг на друга. Такой случай образования глобулярных цепных молекул может реализоваться в синтетических полимерах. [10]
Если принять, что число водородных связей равно двум, то получается, что экспериментальное значение Q2 превышает расчетное на 40 ед. У высших н-спиртов это превышение возрастает, что связано с изгибанием, свертыванием молекул и образованием пространственных структур. [11]
В некоторых случаях под сольватацией понимают стабилизацию, определяемую взаимодействием между растворителем и растворенным веществом. В такой ситуации говорят о стабилизации растворенного вещества растворителем, В более широком смысле иногда сольватацией называют всякие эффекты, приводящие к стабилизации молекулы, например свертывание молекулы с длинной цепью в паровой фазе и сольватацию ( стабилизацию) про-тивоионами с образованием ионных пар в средах с низкой диэлектрической проницаемостью. [12]
Эксперименты показали, что после восстановления нативной рибонуклеазы, взятой в концентрации менее 0 1 %, и последующего ее окисления около 70 % окисленного материала оказывается растворимым и активность этой растворимой фракции составляет от 80 до 100 % активности нативного фермента. Осадок состоит, вероятно, из молекул, соединенных межмолекулярными связями. Окисление в присутствии мочевины не приводит к появлению активного продукта. Эти факты свидетельствуют о том, что характер свертывания молекулы белка предопределен ее аминокислотной последовательностью. [13]
Страницы: 1