Сводка - значение
Cтраница 4
Таким образом, когда окисление метана не лимитировано реакцией зарождения, величина / аф не должна существенно выходить за пределы 60 - 70 ккал, равно как и Е, для реакции окисления НСНО. К сожалению, существующие экспериментальные данные о температурной зависимости скорости окисления формальдегида весьма противоречивы. В сводке значений Е для этого процесса, приведенной в работе Шесра [121], они заключены в пределах 17 6 - 29 4 ккал. [46]
 |
Определение Яоф медленного окисления этана в смеси 2С2Нг, - О. [47] |
Таким образом, когда окисление метана не лимитировано реакцией зарождения, величина E3 не должна существенно выходить за пределы 60 - 70 ккал, равно как и Е для реакции окисления НСНО. К сожалению, существующие экспериментальные данные о температурной зависимости скорости окисления формальдегида весьма противоречивы. В сводке значений Е для этого процесса, приведенной в работе Шеера [121], они заключены в пределах 17 6 - 29 4 ккал. [48]
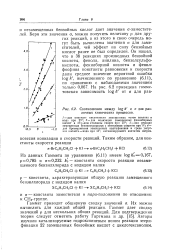 |
Соотношения между log k и а для различных химических процессов. [49] |
Гаммет приводит обширную сводку значений а. Гаммет дает сводку значений р для нескольких общих реакций. Авторы изучили катализируемые гидроксониевым ионом реакции этери-фикации 22 замещенных бензойных кислот с циклогексанолом. [50]
В 30 - х годах становится все более общепринятым проводить термодинамическое исследование реакции, предполагаемой к постановке или уже используемой на производстве, с целью выяснения наиболее благоприятных условий для достижения хорошего-выхода. Это сопровождается дальнейшим расширением справочных данных по термодинамическим свойствам веществ и термодинамическим параметрам реакций. Выходит первая большая критически составленная сводка значений теплот образования неорганических соединений, выпущенная Биховским и Россини 17, в которой данные разных авторов приведены в основном в единую систему. [51]
В 30 - х годах становится все более общепринятым проводить термодинамическое исследование реакции, предполагаемой к постановке или уже используемой на производстве, с целью выяснения наиболее благоприятных условий для достижения хорошего выхода. Выходит первая большая критически составленная сводка значений теплот образования неорганических соединений, выпущенная Биховским и Россини 17, в которой данные разных авторов приведены в основном в единую систему. [52]
 |
Зависимость пределов взрываемости от природы инертного компонента в системе СН4 воздух ( Аг, Не, N2, Н2О, COj при нормальных условиях. [53] |
Еще Эджертон [216] отметил, хотя не вполне определенно и не объясняя, что температура горения ряда смесей и на нижнем и на верхнем пределе взрываемости сохраняет приблизительно постоянное значение. В табл. 6 дана сводка значений ТЬкр, соответствующих наиболее достоверным экспериментальным значениям птт-яех бедных воздушных смесей ряда уг-леродсодержащих горючих. [54]
Еще Эджертон [216] отметил, хотя не вполне определенно в не объясняя, что температура горения ряда смесей и на нижнем и на верхнем пределе взрываемости сохраняет приблизительно постоянное значение. В табл. 6 дана сводка значений Гькр, соответствующих наиболее достоверным экспериментальным значениям nminJtra бедных воздушных смесей ряда уг-леродсодержащих горючих. [55]
 |
Зависимость пределов взрываемости от природы инертного компонента в системе СН4 воздух ( Аг, Не, N2, H2O, С02 при нормальных условиях. [56] |
Еще Эджертон [216] отметил, хотя не вполне определенно и не объясняя, что температура горения ряда смесей и на нижнем и на верхнем пределе взрываемости сохраняет приблизительно постоянное значение. В табл. 6 дана сводка значений ГЬКР, Соответствующих наиболее достоверным экспериментальным значениям Лтш я с бедных воздушных смесей ряда уг-леродсодержащих горючих. [57]
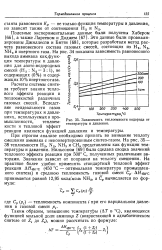 |
Зависимость теплоемкости водорода от температуры и давления. [58] |
При строгом анализе необходимо принять во внимание теплоту смешения аммиака с неконвертированным синтез-газом. На рис. 35 - 38 теплоемкости Н2, N2, NH3 и СН4 представлены как функции температуры и давления. Нильсоном [69] была сделана сводка значений теплового эффекта реакции при 500 С, полученных различными авторами. [59]
К) слабо влияет на коэффициент захвата, пока мощность охлаждающей системы достаточна для поддержания нриопаверхностей при указанных выше температурах. Последующие измерения, проведенные Брауном и др. [5] и Арнольдом др. [6], показали, что коэффициент захвата аргона и азота при температурах газа выше 1500 К равномерно уменьшается с увеличением температуры газа, даже когда температура криоловерхности ниже 20 К; при температуре газа около 2500 К. В табл. 10.1 представлена сводка намеренных значений коэффициентов захвата, которые MOiryr быть использованы при определении характеристик криогенных откачивающих систем для атмосферных газов. [60]
Страницы: 1 2 3 4 5