Свойство - донор
Cтраница 1
Свойства донора значительно зависят от свойств акцептора. Например, найдено ( Р. И. Нидзиельски, Р. С. Драго и др.), что ( С2Н5) 2О является более сильным донором по отношению к фенолу ( энтальпия образования аддукта АЯобр - 5 ккал / молъ), чем ( C2H5) 2S ( АД обр - 4 6 ккал / молъ), но ( C2HB) 2S является лучшим донором по отношению к иоду ( A. По-видимому, в этих системах деформируемый ( С2НБ) 28 более сильно взаимодействует с деформируемым иодом, чем полярный ( С2Н5) 20, а последний более сильно взаимодействует с полярным фенолом. Это правило должно быть общим. [1]
Проявляет свойства донора и акцептора фторид-иона. [2]
Растворителем, сочетающим в себе свойства донора водорода и донора электронов, является тетрагидрохинолин. При давлении 7 6 МРа в гексане растворяется 30 - 35 %, а при давлении 15 6 МРа - около 60 % веществ, экстрагируемых хинолином. Эти продукты термически нестабильны, поскольку перегнать удается лишь незначительную их часть, особенно в случае получения водорода при более низком давлении. Следовательно, переход веществ в раствор обусловлен их стабилизацией благодаря, очевидно, гидрированию и межмолекулярному взаимодействию с тетрагидрохинолином и продуктами его превращения - димером тетрагидрохинолина и хинолином, присутствие которых установлено с помощью масс-спектрометрии. При низком давлении водорода часть тетрагидрохинолина остается в нерастворившемся остатке. [3]
Наличие простой монотонной зависимости между свойствами доноров или акцепторов, имеющих постоянную величину и знак заряда, и кислотностью подтверждается также огромным числом работ из области ионного катализа. [4]
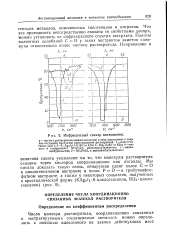 |
Инфракрасный спектр поглощения. [5] |
Что эта пригодность непосредственно связана со свойствами донора, можно установить из инфракрасного спектра экстракта. Полосы валентных колебаний С О у таких экстрактов заметно сдвинуты относительно полос чистого растворителя. [6]
Неподеленная электронная пара азота сообщает молекуле аммиака свойства донора. Поэтому для аммиака характерна способность образовывать связи по донорно-акцепторному механизму. Комплексные соединения, содержащие молекулы аммиака, называют аммиакатами. [7]
Неподеленная электронная пара азота сообщает молекуле аммиака свойства донора. Поэтому для аммиака характерна способность образовывать связи по донор но-акцепторнму механизму. Комплексные соединения, содержащие молекулы аммиака, называют аммиакатами. [8]
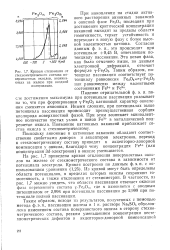 |
Кривая отклонения от стехиометрического состава поверхностных окислов, возникающих на железе при анодной поляризации. [9] |
Поскольку анионные и катионные вакансии обладают соответственно свойствами доноров и акцепторов электронов, переход к стехиометрическому составу приводит к акцепторно-донорной компенсации у окисла, благодаря чему концентрация Fe2 ( или концентрация З - электронов) в окисле уменьшается. [10]
Общеизвестно, что аммиак и его производные проявляют свойства донора гораздо энергичнее, чем окислы азота. [11]
Подобно сиднониминам, производные других мезо-ионных соединений проявляют выраженные свойства доноров оксида азота и соответствующие биологические эффекты. Это - оксатриазолиевые производные 1 - 3, оказавшиеся весьма эффективными ингибиторами агрегации тромбоцитов, способные устойчиво снижать артериальное давление в модельных опытах на животных и проявляющие противоастматический эффект. [12]
Акцепторные свойства сильных акцепторов электронной пары не зависят от свойств донора иона хлора, но слабые акцепторы, такие, как хлорид титана ( 1У) или ZnCl2, сильнее взаимодействуют с ковале нтными донорами иона хлора, чем с ионными хлоридами. [13]
Как было показано выше, в угле присутствуют фрагменты, проявляющие свойства донора водорода, и он также может служить передатчиком водорода. [14]
Для соединений этого типа, у которых группа X обладает свойствами донора электронов, возможно образование внутри - и межмолскулярных координационных связей. В соответствии с этим многочисленные известные соединения, отвечающие эмпирической формуле RZnX ( где X - галоген, OR1, NR21, SR1 или PR21), обладают чрезвычайным разнообразием структур. Два примера этих соединений показаны ниже. [15]
Страницы: 1 2 3 4