Свойство - анион
Cтраница 1
Свойства аниона, нейтральной молекулы или иона металла часто можно намеренно изменить в результате комплексообразо-вания с ионом металла, которое приводит к появлению аналитически полезных форм. [1]
Свойства анионов в отношении коагуляции желатины определяются лиотропным рядом Гофмейстера ( стр. [2]
Какие свойства анионов положены в основу их аналитической классификации. [3]
Сопоставление свойств элементных анионов ( хлорид -, сульфид-ионов и др.) с кислородсодержащими сложными анионами ( сульфат -, фосфат-ионов и др.) невозможно без учета их особенностей. Поэтому ионы S2 - и SO - довольно резко отличаются по растворимости их серебряных, бариевых и ртутных солей. [4]
В дальнейшем рассматриваются свойства аниона кислой соли двухосновной кислоты. Свойства аниона НА довольно сложны. Кислую соль можно рассматривать как кислоту, в которой не все водородные ионы замещены на металл. [5]
Ярко выраженные нуклеофилыше свойства фосфидных анионов демонстрирует последовательность реакций превращения ж-толилиодида в фенил-л - толилфосфин. Эти реакции представляют собой нуклеофильное замещение, а не образование арина, как в случае взаимодействия арилгалогенидов с амид-ионами. [6]
Комплекс может обладать свойствами аниона, катиона или быть нейтральным. [7]
 |
Сродство к проточу различных молекул и ионов. [8] |
Эта величина влияет на свойства анионов и, в частности, на взаимное вытеснение ионов из органической фазы в водную. [9]
В щелочной среде краситель обладает свойством аниона и образует соль с металлом, а в кислой - катиона и образует соль с кислотой. [10]
В табл. 9, 10 приведены свойства анионов I, II и III аналитических групп и соединений, образуемых ими с некоторыми реагентами. [11]
Образование этих соединений подтверждает общеизвестную аналогию свойств анионов галогенов и циановой и тиоциановой кислот. [12]
Дальнейшее исследование ведут основываясь на изученных ранее свойствах анионов. По универсальной индикаторной бумаге определяют рН раствора. В кислом растворе ( рН 2) не может быть карбонат -, сульфит -, тиосульфат - и сульфид-ионов, но могут присутствовать хлорид -, сульфат -, нитрат - и фосфат-ионы. [13]
 |
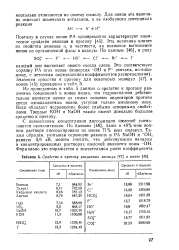
Изотермы повышения поверхностного и пограничного натяжения Дст, а также значения - фн. з в растворах CsF и KF. [14] |
В связи с изложенным значительный интерес представляло исследование электрокапиллярных свойств анионов другого типа, например F - - иона. Нами были сняты емкостные данныедля KF и CsF в широком диапазоне концентраций. С теми емкостными данными для KF, которые были приведены в [18], согласие было хорошим. Емкостные кривые для CsF по форме и расположению аналогичны кривым KF. [15]
Страницы: 1 2 3 4