Свойство - серная кислота
Cтраница 1
 |
Некоторые физические свойства безводной серной кислоты. [1] |
Свойства серной кислоты как растворителя подробно описаны в исчерпывающих обзорных статьях; здесь же будут кратко изложены только некоторые характерные особенности химии координационных соединений в этом растворителе. [2]
Свойство серной кислоты жадно поглощать воду применяется для осушки газов и обезвоживания в целом ряде химических процессов. В связи с разрушительным действием на некоторые органические вещества серная кислота используется для очистки нефтепродуктов, растительных масел и пр. [3]
Свойства серной кислоты настолько разнообразны, что она применяется практически в каждой стадии синтеза алкилбензолсульфонатов, и прежде всего, разумеется, в стадии сульфирования. Ее используют также в стадии алкилирования и даже для очистки непредельных углеводородов, предназначенных для алкилирования. [4]
Свойствам серной кислоты, олеума и промежуточным продуктам их производства ( SO2 и SO3) в разных странах посвящены сотни работ. Результаты наиболее достоверных фундаментальных исследований отражены в Справочнике сернокис-лотчика под редакцией проф. [5]
Эти свойства серной кислоты положительно влияют на интенсификацию нефтевытеснения, повышая нефтеотдачу пластов. [6]
Какие свойства серной кислоты вам известны. [7]
Какие свойства серной кислоты позволяют применять ее для производства кислот. [8]
Это свойство серной кислоты используют также в нефтеперерабатывающей промышленности для очистки бензина, керосина и других нефтяных масел от таких примесей, которые при хранении нефтепродуктов осмо-ляются и загрязняют их. В процессе очистки эти примеси взаимодействуют с серной кислотой с образованием эфиров кислоты и продуктов полимеризации, нерастворимых в очищаемых продуктах. [9]
Эти свойства серной кислоты объясняются тем, что над кислотой ниже 98 3 % - ной концентрации ( слабый моногидрат) находятся пары воды, а цад кислотой выше 98 3 % - ной концентрации ( крепкий моногидрат) находится серный ангидрид. Поэтому при обработке газовом смеси, содержащей серный ангидрид, слабым моногидратом часть серного ангидрида соединяется с парами воды и образуется туман серной кислоты. Этот туман мало улавливается в обычной абсорбционной аппаратуре и в основном выбрасывается газовым потоком в атмосферу. В этом олучае в выхлопной трубе наблюдается туман, или, как принято говорить абсорбер газит. Чем слабее моногидрат ( чем ниже концентрация кислоты) и чем выше его температура, тем больше паров воды выделяется из серной кислоты, тем больше образуется тумана и TieM больше потери. [10]
 |
Влияние концентрации кислоты и температуры на полноту поглощения серного ангидрида. [11] |
Эти свойства серной кислоты объясняются тем, что над кислотой, содержащей менее 98 3 % моногидрата, находятся главным образом пары воды и незначительное количество паров серной кислоты. Над кислотой, содержащей более 98 3 % H2SO4, в парах находится в основном серный ангидрид. [12]
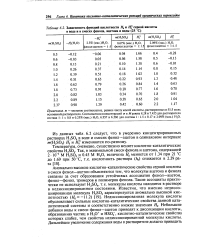 |
Зависимость функций кислотности Я0 и Я / серной кислоты в воде и в смесях фенола, ацетона и воды ( 25 С. [13] |
Аномально высокие кислотно-каталитические свойства серной кислоты в смеси фенол-ацетон объясняются тем, что молекулы ацетона и фенола связаны за счет образования устойчивых ассоциатов фенол-ацетон, фенол-фенол, тримеров и полимеров фенола. Такие ассоциаты практически не используют H2SO4, т.е. молекулы кислоты находятся в растворе в недиссоциированном состоянии. Небольшие добавки воды к смеси фенол-ацетон приводят к диссоциации кислоты, образованию частиц в Н3О и HSO4 -, кислотно-каталитические свойства которых слабее, чем свойства недиссоциированной молекулы кислоты. [14]
Помимо водуотнимающих свойств серной кислоты ( точно так же, как и смеси ледяной уксусной кислоты с уксусным ангидридом), присутствие серной кислоты способствует усилению нитрующего действия азотной кислоты при одновременном уменьшении ее окислительных свойств. [15]
Страницы: 1 2 3 4