Свойство - атом - элемент
Cтраница 2
Положением элемента в таблице Д. И. Менделеева определяется его валентность - свойство атомов элемента образовывать химическую связь. Обычно номер группы указывает на число электронов, которые могут участвовать в образовании химической связи. Такие электроны называются валентными. Однако у элементов побочных подгрупп валентными являются электроны не только внешних, но и предпоследних уровней. В этом и состоит основное различие в свойствах элементов главных и побочных подгрупп. В табл. 7 приведены валентности, наиболее часто проявляемые элементами. Максимальная валентность, как правило, равна номеру группы. [16]
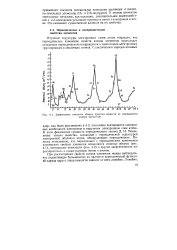 |
Зависимость атомного объема простых веществ от порядкового. [17] |
Изучение структуры электронных слоев атома показало, что периодическое изменение свойств атомов элементов происходит вследствие периодического возвращения к однотипным электронным группировкам в оболочках атомов. [18]
Согласно теории строения и всем имеющимся эмпирическим данным, химические свойства соединений зависят от свойств образующих их элементов. Какое же свойство атомов элемента является основным, определяет все остальные свойства атома, а значит, и элемента, позволяет отличать атомы одного элемента от атомов другого. Исследования, проведенные до установления сложной структуры атома, показали, что таким решающим, главным свойством является атомный вес элемента. Именно на этом фундаментальном свойстве, связанном с самой природой элемента, должна быть и основана, по мнению Менделеева, научная система элементов. [19]
Второе издание ( 1 - е вышло в 1975 г.) дополнено новым материалом. Все таблицы с характеристикой свойств атомов элементов и простых веществ представлены Б единицах СИ. [20]
Как известно, под валентностью понимают свойство атомов элемента присоединять определенное число атомов других элементов. [21]
Как это следует из самой формулировки периодического закона, он относится к свойствам элементов. Однако, поскольку свойства простых тел зависят, главным образом, от свойств атомов элементов, их образующих, постольку периодичность в подавляющем большинстве случаев проявляется и для простых тел. [22]
В связи с тем, что между нуклонами действуют качественно иные силы, чем в электронной оболочке атомов, емкость ядерных энергетических уровней иная, чем емкость электронных уровней. Конечно, и периодичность изменения свойств ядер имеет другой характер по сравнению со свойствами атомов элементов, обусловливаемых строением их электронной оболочки. [23]
Эга черта диалектического материализма лучше всего характеризуется звездностью периодической системы, то есть закономерным изменением свойств атомов элементов, просгых тел и сложных соединений при рассмотрении их: по периоду ( слева направо), по подгруппе ( сверху вниз) и, наконец, по диагонали. [24]
Эта черта диалектического материализма лучше всего характеризуется звездностью периодической системы, то есть закономерным изменением свойств атомов элементов, простых тел и сложных соединений при рассмотрении их: по периоду ( слева направо), по подгруппе ( сверху вниз) и, наконец, по диагонали. [25]
Дать единое современное определение валентности довольно трудно. Валентность связана с порядковым номером элементов в периодической системе. Это свойство атомов элементов соединяться друг с другом, образуя молекулу. [26]
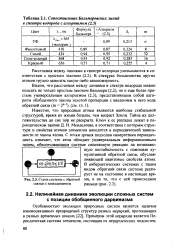 |
Сопоставление Бальмеровских линий в спектре водорода с алгоритмом.| Схема системы с обратной связью с запаздыванием. [27] |
Известно, что природные атомы являются наиболее стабильной структурой, время их жизни больше, чем возраст Земли. Тайна их долгожительства до сих пор не раскрыта. Ключ к ее разгадке лежит в периодическом законе Д. И. Менделеева, в соответствии с которым структура и свойства атомов элементов находится в периодической зависимости от массы атома. С точки зрения подходов синергетики периодичность означает, что атом обладает универсальным информационным полем, обеспечивающим системе спонтанную реакцию на возникающую нестабильность с помощью кумулятивной обратной связи, обуславливающей квантовые свойства атома. [28]
Страницы: 1 2