Свойство - переходный металл
Cтраница 1
Свойства переходных металлов в большой степени определяются относительными величинами потенциала кристаллического поля и энергии спин-орбитального взаимодействия. Как мы видели в предыдущем разделе, эти два типа взаимодействия влияют на орбитальное вырождение в противоположных направлениях. [1]
Ряд свойств переходных металлов обусловливается частичным переходом s - электронов в зону незанятых ( п - 1) с. Указанным переходом объясняется прежде всего низкая электрическая проводимость переходных металлов по сравнению с металлами подгруппы меди. Так как распределение электронов между - s - и d - зонами при их перекрывании зависит от температуры, давления и посторонних включений. [2]
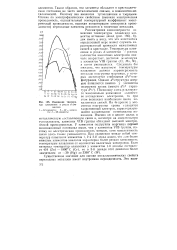 |
Изменение температур плавления в рядах d - эле. [3] |
Существенное значение для оценки металлохимических свойств переходных металлов имеет внутренняя периодичность. [4]
Они позволяют качественно объяснить многие свойства переходных металлов; следует учитывать, что среди стабильных конфигураций максимально устойчива d3, вносящая наибольший вклад в организацию химической связи. [5]
 |
Гибридизация орбиталей и пространственное расположение связей. [6] |
Образование координационных связей часто считается свойством переходных металлов, однако этот тип связи никоим образом не ограничен этими элементами. Такие элементы главных групп, как бор, алюминий, кремний и олово, образуют много координационных соединений. [7]
Какие систематические закономерности обнаруживаются в свойствах переходных металлов на основании изложенных выше фактов. [8]
Отметим еще одно важное обстоятельство, существенно влияющее на закономерности изменения свойств переходных металлов. Дело в том, что у элементов ряда Sc-Zn ( вставная декада 4-го периода) заполняющаяся 3з ( - оболочка появляется впервые и является кайносимметричной. Вследствие этого наблюдается более прочная связь Sd-электронов с ядром, чем у 4d - и 5 -элементов. Это наиболее наглядно иллюстрируется значениями 3-го потенциала ионизации, отвечающего отрыву первого d - электрона. В дальнейшем в рядах rf - металлов эта закономерность так четко не прослеживается, потому что на нее накладывается лантаноидное сжатие. Подобное же положение характерно и для 4 / - элементов по сравнению с остальными / - элементами, поскольку 4 / - оболочка также является кайносимметричной. Таким образом, первый ряд d - эле-ментов и первый ряд / - элементов также обладают своеобразием по сравнению со своими более тяжелыми аналогами, подобно элементам 2-го периода по сравнению с типическими р-элементами 3-го периода. [9]
Отметим еще одно важное обстоятельство, существенно влияющее на закономерности изменения свойств переходных металлов. Дело в том, что у элементов ряда Sc - Zn ( вставная декада 4 - - го периода) заполняющаяся 3 / - оболочка появляется впервые и является кайносимметричной. Это наиболее наглядно иллюстрируется значениями 3-го потенциала ионизации, отвечающего отрыву первого d - электрона. В самом деле, сравнивая эти величины для элементов начала декад ( Sc - Y - La), можно видеть, что хотя сверху вниз потенциалы ионизации и уменьшаются, это уменьшение немонотонно: при переходе от Sc к Y 3 - й потенциал ионизации уменьшается на 4 В, а от Y к La - всего на 1 В. В дальнейшем в рядах d - металлов эта закономерность так четко не прослеживается, потому что на нее накладывается лантаноидное сжатие. Подобное же положение характерно и для 4 / - элементов по сравнению с остальными / - элементами, поскольку 4 / оболочка также является кайносимметричной. Таким образом, первый ряд rf - элементов и первый ряд / - элементов также обладают своеобразием по сравнению со своими более тяжелыми аналогами, подобно элементам 2-го периода по сравнению с типическими р-элементами 3-го периода. [10]
Такая общая концепция классификации связей пройдет через весь этот раздел, хотя детали могут меняться в зависимости от природы органических лигандов и свойств переходных металлов. [11]
Из-за небольшого размера атомов С и N по сравнению с атомами переходных металлов неметалл занимает промежуточные участки, образующиеся при плотной упаковке атомов переходных металлов, и значительно модифицирует свойства исходного переходного металла. Некоторые из этих изменений обсуждаются в данном разделе. [12]
Высокая температура плавления и низкая сжимаемость тория обусловлены тем, что, помимо двух электронов, занимающих уровни 7s, у него имеется еще два внешних электрона на уровнях 6d, и это придает торию свойства переходного металла подгруппы IVA. У следующих элементов - протактиния, урана и нептуния-температуры плавления резко понижаются, что указывает на уменьшение сил связи в решетке этих элементов, однако, как следует из фиг. Это противоречие аналогично наблюдаемому у последних переходных элементов каждой группы. При этом предпочтение опять-таки следует отдать данным по сжимаемости, которая зависит только от свойств вещества в твердом состоянии. Поскольку различия в энергиях 5 / -, Qd - и Ts-орбиталей весьма незначительны, то у первых членов актинидного ряда важную роль в процессе образования связей должны играть, по всей вероятности, 5 / - орбитали, которые могут гибри-дизироваться с Gd - и 7х - орбиталями. [13]
Высокая температура плавления и низкая сжимаемость тория обусловлены тем, что, помимо двух электронов, занимающих уровни Is, у него имеется еще два внешних электрона на уровнях 6d, и это придает торию свойства переходного металла подгруппы IVA. У следующих элементов - протактиния, урана и нептуния -, температуры плавления резко понижаются, что указывает на уменьшение сил связи в решетке этих элементов, однако, как следует из фиг. Это противоречие аналогично наблюдаемому у последних переходных элементов каждой группы. При этом предпочтение опять-таки следует отдать данным по сжимаемости, которая зависит только от свойств вещества в твердом состоянии. Поскольку различия в энергиях 5 / -, 62 - и Ts-орбиталей весьма незначительны, то у первых членов актинидного ряда важную роль в процессе образования связей должны играть, по всей вероятности, 5 / - орбитали, которые могут гибри-дизироваться с 6d - и Ts-орбиталями. [14]
При образовании кристаллических решеток переходных металлов ns - и ( п - 1) й-электронные подуровни расщепляются в зоны, которые перекрывают друг друга; s - и d - электроны различным образом распределяются в зонах. Ряд свойств переходных металлов обусловливается частичным переходом ns - электронов в зону незанятых ( п - - состояний. Указанным переходом объясняется прежде всего низкая электропроводность переходных металлов по сравнению с непереходными металлами подгруппы меди. Так как распределение электронов между s - и d - полосами при их перекрывании зависит от температуры, давления и посторонних включений, а изменение электронного распределения в твердом теле может изменить кристаллическую решетку, то многие переходные металлы полиморфны. [15]
Страницы: 1 2