Свойство - молекула - вода
Cтраница 1
Свойства молекул воды заслуживают внимания, ибо вода, хоть и не относится непосредственно к органическим веществам, составляет главную часть всех живых организмов. [1]
Многие свойства молекулы воды установлены в результате анализа полосатых спектров испускания или поглощения молекул воды в газовой фазе. [2]
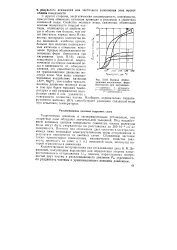 |
Кривые обезвоживания моноионных форм бентонитов при нагревании. [3] |
С другой стороны, энергетическая неоднородность поверхности, присутствие обменных катионов приводят к различию в свойствах связанной воды. Свойства молекул воды, связанных обменными ионами поверхности твердой частицы, отличаются от свойств воды в объеме тем больше, чем выше плотность заряда иона. В глинистых минералах количество воды, связанной наиболее прочно, больше при наличии поливалентных катионов в обменном комплексе. [4]
Таким образом, взаимодействие истинных и потенциальных электролитов с водой является химическим, приводящим к разрушению ионных или молекулярных кристаллов или молекул и образованию гидратированных ионов. Для реализации электролитической диссоциации особое значение имеют донорно-акцепторные свойства молекулы воды. [5]
Обнаружено, что даже при снижении средней, макроскопической диэлектрической проницаемости в ЗО раз и более путем введения в воду неорганических солей микроскопическая полярность меняется очень слабо в противоположность сильному влиянию добавок спиртов. Низкая макроскопическая диэлектрическая проницаемость концентрированных растворов солей отражает усредненные свойства молекул воды, связанных с ионами, и свободных молекул воды. Для ближних взаимодействий между ионами в ионных парах и на поверхности раздела наиболее важна полярность ближайшего окружения ( в сольвагной оболочке), и присутствие гидратированных ионов, по-видимому, влияет лишь в незначительной мере. [6]
Что касается пряного спектроскопического подтверждения существования Hjd в разбавленных растворах сильных кислот, то оно затруднительно. Белл [38] указал, что характерные свойства гид-роксониевого иона будут незначительно отличаться от свойств молекул воды, всегда присутствующей в избытке, и что скорость обмена протонами между молекулами воды может быть так велика, а время жизни Hj О настолько мало, что свойства Н3 О будут совершенно незаметны, особенно в методе ИКС. Тем не менее ряд авторов при исследовании водных растворов кислот полосы, обнаруженные в области 2900, 1700, 1200 см 1, отнесли, на основании колебательных спектров HjO кристаллического, к иону НзО в водном растворе. [7]
Этот механизм представляет собой специфический кислотный-общеосновной катализ реакции в прямом направлении. В обратном направлении катализатор должен действовать, отдавая протон уходящей гидроксильной группе, с тем чтобы частично придать ей свойства молекулы воды и тем самым увеличить ее способность к удалению. Это и есть непосредственный общекислотный катализ. [8]
Уже из этих примеров видно, какие различные функции в структуре вещества могут выполнять молекулы воды и продукты ее диссоциации. Весьма вероятно, что в большом разнообразии свойств веществ, содержащих воду, которые обычно объясняются исключительно строением самих этих веществ, в действительности не меньшую роль играют свойства молекулы воды. Поэтому при изучении структуры и реакционной способности вещества факт обнаружения в нем молекул воды, продуктов ее диссоциации или каких-либо их комплексов, иначе говоря обнаружение в веществе группировок, построенных из атомов водорода и кислорода ( OmHn-группировок) - будем называть их оксигидрильными группировками - еще ничего не говорит о их свойствах, которые могут оказаться самыми различными и часто весьма неожиданными. Иллюстрацией разнообразия свойств ОН-групп могут служить хорошо известные свойства ОН-групп кислот и щелочей. [9]
Движущиеся частицы газа мы называем молекулами. Название это пришло из химии, где оно означает мельчайшие частицы вещества, которые могут еще существовать самостоятельно. Так, молекула воды, Н2О, дает Два атома водорода и один кислорода, свойства которых отличны от свойств молекулы воды. Предоставленные самим себе отдельные атомы группируются в пары Н2 и 02 - молекулы газов водорода и кислорода. В кинетической теории газов мы имеем дело с молекулами и предполагаем, что они не расщепляются при соударениях. Кроме того, мы считаем, что молекулы действуют друг на друга лишь в момент соударения; когда они оказываются достаточно близко друг к другу, они испытывают действие отталкивающей силы, но на очень короткое время. В этом фактически и заключается соударение. [10]
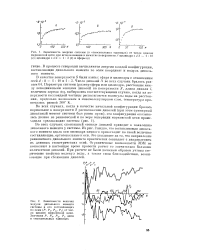 |
Зависимость энергии системы ( в относительных единицах от числа циклов марковской цепи при использовании в качестве поверхности Л цилиндра с il / h - ( я. цилиндра с cl / h 1. 3 ( б и сферы ( в. [11] |
Во всех случаях спонтанный повал диполей приводит к появлению дипольного момента у системы. Из рис. 2 видно, что составляющая диполь-иого момента вдоль оси цилиндра намного превосходит по своей величине составляющие, ортогональные к оси. Это указывает на то, что направление равновесного дипольного момента практически совпадает с направлением их длинных геометрических осей. Ограниченные возможности ЭВМ не позволяют в настоящее время провести расчет со значительно большим количеством диполей. При расчете не были должным образом учтены сте-рические свойства молекул воды, а также силы близкодействия, возникающие при сближении диполей. [12]
 |
Структура молекулы воды. [13] |
Первостепенную роль в теории колебательных спектров играют свойства симметрии и операции симметрии молекул. Поскольку атомы в молекулах ( точнее, ядра атомов) расположены в определенном порядке и образуют вполне определенную конфигурацию, то, очевидно, можно говорить о той или иной симметрии молекул. Характеризуется симметрия молекул так же, как и любое другое геометрическое тело, одним или несколькими элементами симметрии, а именно осью, плоскостью и центром симметрии. Каждому элементу симметрии соответствует операция симметрии - такое перемещение системы ( отражение или вращение), которое не приводит к изменению конфигурации и свойств молекулы. Зеркальное отражение всех атомов в этих плоскостях не меняет ни структуры, ни свойств молекулы воды. Операция отражения во второй плоскости меняет местами атомы водорода. [14]
Страницы: 1