Свойство - окись - алюминий
Cтраница 2
Одним из наиболее часто применяемых адсорбентов является окись алюминия, на которой удается хроматографи-чески разделить весьма широкий круг смесей веществ как из полярных, так и аполярных растворителей. Это свойство окиси алюминия как адсорбента определяется тем, что она обладает амфотерным характером. [16]
Таким образом, в большинстве работ указывается на то, что обработка поверхности окиси алюминия содержащими фтор соединениями ( максимальная концентрация фтора, составляет около 6 вес. Изменение свойств окиси алюминия при фторировании объясняется [33, 35] увеличением концентрации на поверхности протонных кислотных центров. [17]
Адсорбционная способность поверхностноактивной окиси алюминия возрастает еще и вследствие того, что посторонние ионы располагаются не только на поверхности окиси, но частично поверхностно внедряются в ее решетку, вытесняя ионы алюминия в раствор. Эта способность к ионному обмену обозначается как пермутоидное свойство окиси алюминия, и та часть адсорбции, которая сводится к этому явлению, называется химической адсорбцией. Фрике ( Fricke, 1948 - 1950) показал, что способность поверхностноактивной окиси алюминия к ионному обмену не обусловлена содержанием в последней щелочей, как это первоначально предполагалось. Действительно, при применении А1203, содержащей щелочи ( например, мерковской А1203, полученной по Брокману), щелочные ионы принимают участие в обмене. [18]
Адсорбционная способность поверхностноактивной окиси алюминия возрастает еще и вследствие того, что посторонние ионы располагаются не только на поверхности окиси, но частично поверхностно внедряются в ее решетку, вытесняя ионы алюминия в раствор. Эта способность к ионному обмену обозначается как пермутоидное свойство окиси алюминия, и та часть адсорбции, которая сводится к этому явлению, называется химической адсорбцией. Фрике ( Fricke, 1948 - 1950) показал, что способность поверхност-поактивной окиси алюминия к ионному обмену не обусловлена содержанием в последней щелочей, как это первоначально предполагалось. Действительно, при применении А12О3, содержащей щелочи ( например, мерковской А1203, полученной по Брокмаиу), щелочные ионы принимают участие в обмене. [19]
Адсорбционная способность поверхностноактивной окиси алюминия возрастает еще ж вследствие того, что посторонние ионы располагаются не только на поверхности окиси, но частично поверхностно внедряются в ее решетку, вытесняя ионы алюминия в раствор. Эта способность к ионному обмену обозначается как пермутоидное свойство окиси алюминия, и та часть адсорбции, которая сводится к этому явлению, называется химической адсорбцией. Фрике ( Fricke, 1948 - 1950) показал, что способность поверхностноактивной окиси алюминия к ионному обмену не обусловлена содержанием в последней щелочей, как это первоначально предполагалось. Действительно, при применении А12О3, содержащей щелочи ( например, мерковской А1203, полученной по Брокману), щелочные ионы принимают участие в обмене. [20]
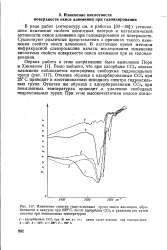 |
Изменение спектра гидроксильных групп окиси алюминия, обработанной в вакууме при 800 С, после адсорбции СС14 и удаления его путем откачки при повышенных температурах. [21] |
В ряде работ ( литературу см. в работах [30-36]) установлено изменение свойств кислотных центров и каталитической активности окиси алюминия при галоидировании ее поверхности. Существуют различные представления о причинах такого изменения свойств окиси алюминия. В настоящее время методом инфракрасной спектроскопии начаты исследования изменения кислотных свойств поверхности окиси алюминия при ее галоидировании. [22]
В нашей работе [1] показано, что изомеризующая активность силикагеля может быть подавлена при его обработке щелочами. Тот же прием использован нами с целью модификации свойств окиси алюминия. Нами изучена дегидратация первичного гептилового спирта в присутствии у - А1203 обработанной различными количествами гидроокисей лития и калия. [23]
Если предположить, что в образце 6 все поверхностные ОН-группы замещены на фтор, то возрастание активности от образца 2 к 6 показывает, что наличие поверхностных ОН-групп для дальнейшего формирования каталитически активных центров не обязательно. Однако в литературе имеются указания, что возникновение или усиление крекирующих свойств окиси алюминия [17] связано с протонизацией поверхностных гидроксильных групп близко расположенными атомами галоида. С увеличением количества фтора в образцах 17 - 22 уменьшается концентрация гидроксильных групп. Активность возрастает, однако максимум активности отсутствует. Таким образом, активность зависит от содержания фтора в катализаторах; но возникновение крекирующих свойств нельзя объяснить протонизацией атомами фтора как поверхностных ОН-групп окиси алюминия, так и ОН-групп в гидроксофторидах алюминия. [24]
Как известно 12 13, активная окись алюминия является кислотным катализатором, широко применяемым в промышленных процессах. Из хроматограммы катализата видно ( рис. 2), что при использовании окиси алюминия помимо капролактама образуется значительное количество побочных продуктов. Наличие воды в катализате служит подтверждением дегидратирующих свойств окиси алюминия и в этом процессе. В отходящих газах отмечено значительное количество аммиака. [25]
Гидроокись алюминия при нагревании довольно трудно теряет воду. Следы воды удаляются при очень сильном прокаливании. Наоборот, окись алюминия способна поглощать воду из вюздуха, которая постепенно может из адсорбированной переходить в химически связанную. Это свойство окиси алюминия сохраняется в катализаторе. Приготовленные на основе гидроокиси алюминия катализаторы обладают некоторой гигроскопичностью, в результате чего они могут увлажняться и терять свою активность. Так, алюмомолиб-деновый катализатор после прокаливания при 650 С, находясь на воздухе, довольно быстро поглощает влагу. Поэтому влажность катализаторов, осажденных на гидроокиси алюминия, определяют при тех же температурах, при которых удаляется остаток воды. Как предусмотрено техническими условиями, содержание воды в алюмо-силикатном катализаторе определяют при 800 С, а алюмомолибде-нового - при 650 С. При этом вместе с удалением воды происходит некоторое разложение катализатора с удалением в основном его органических примесей. [26]
Во-вторых, наличием подобного диагонального направления в системе Менделеева легко объясняется существование определенной связи и сходства между Be, стоящим во II группе второго периода, и А1, стоящим в III группе третьего периода, по диагонали от Be. Однако диагональные отношения в системе элементов играют менее существенную, второстепенную роль по сравнению с главными и наиболее существенными отношениями, которые в системе элементов выражены вертикальным ( в пределах одной группы) и горизонтальным ( в пределах одного ряда) направлениями. Тем не менее диагональные отношения существуют, и их необходимо учитывать. Если в характере окиси бериллия - замечает в связи с этим Менделеев - несмотря на несходство формул, видны многие свойства окиси алюминия, то в характере Li2O видны свойства MgO, а в свойствах В2О3, как известно, много сходного с SiO2 [ 18, стр. [27]
Благодаря развитой поверхности, термической стабильности, повышенной механической прочности и особого строения кристаллической решетки активная окись алюминия находит широкое применение в качестве катализатора и носителя катализаторов различного назначения. В промышленности ее получают сульфатно-алюнинатным способом. Необходимые структурные характеристики и высокая химическая чистота достигаются путем осаждения высокодисперсной гидратированной гидроокиси и ее дальнейшей обработки. Поскольку свойства конечного продукта свнваны со структурой и морфологией исходной гидроокиси [ I, 2 ], то условия ее осаждения, т.е. условия получения осадка грануляции, играют превалирующую роль в формировании таких свойств окиси алюминия, как механическая прочность гранул, насыпная плотность, пористая и кристаллическая структура, и в конечном итоге, - адсорбционная и каталитическая активность. [28]
Страницы: 1 2