Свойство - буферный раствор
Cтраница 1
Свойство буферных растворов сохранять определенное значение рН основано на способности связывать ионы водорода или гидроксила вводимых в них кислот или оснований. [1]
Второе свойство буферных растворов заключается в том, что их рН мало изменяется при добавлении умеренных количеств сильной кислоты или сильного основания. [2]
Приготовление и свойства буферных растворов рассматриваются в гл. Важным свойством буфера является его способность удерживать концентрацию ионов водорода на неизменном определенном уровне. [3]
Для описания свойств буферных растворов важны следующие характеристики. [4]
Разберем, на чем основано свойство буферных растворов, на примере буферной смеси уксусной кислоты и ацетата натрия. [5]
Таким образом, ошибка, благодаря свойствам буферных растворов сохранять приблизительно постоянным рН среды, сравнительно невелика, В рассмотренном случае при приготовлении ацетатного буфер ного раствора добавленная в избытке щелочь увеличила рН раствора всего только на 0 1 по сравнению с заданным. [6]
Таким образом, ошибка, благодаря свойствам буферных растворов сохранять приблизительно постоянным рН среды, сравнительно невелика. В рассмотренном случае при приготовлении ацетатного буферного раствора добавленная в избытке щелочь увеличила рН раствора всего только на 0 1 по сравнению с заданным. [7]
В этой статье дан детальный обзор таких свойств буферных растворов - аминов, как диапазон рН, температурный коэффициент рН, буферное действие, солевой эффект и эффект разбавления. [8]
Смесь угольной кислоты и кислого углекислого натрия также имеет свойства буферного раствора, причем теперь NaHCO3 играет роль соли по отношению к Н2С03, как кислоте. [9]
 |
Пояснение явления расширения и искривления зоны вещества по мере продвижения по колонке. [10] |
Причиной подобного искажения фронта вещества, кстати снижающего разрешение, является свойство буферного раствора двигаться вблизи стенок с повышенной скоростью. [11]
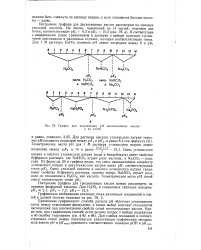 |
График для определения рН многоосновных кислот. [12] |
Смесь углекислого натрия и кислого углекислого натрия ( соды и бикарбоната) имеет свойства буферного раствора, где NaHCO3 играет роль кислоты, a Na2CO3 - роль соли. Из формулы ( 3) и графика видно, что смесь эквивалентных количеств углекислого натрия и двууглекислого натрия имеет рН, соответствующий точке pKz - Смесь угольной кислоты и кислого углекислого натрия также имеет свойства буферного раствора, причем теперь NaHCO3 играет роль соли по отношению к Н2СО3, как кислоте. [13]
Смеси гидро - и дигидрофосфатов ( например, Na2HPO4 NaH2PO4) в водном растворе обладают свойствами буферных растворов ( стр. Эти растворы почти нейтральны ( рН их находится в пределах от 6 до 8), и к ним можно прибавлять в известных пределах кислоты или щелочи без заметного изменения рН раствора. [14]
Смеси гидро - и дигидрофосфатов ( например, Na2HPO4 - fNaH2PO4) в водном растворе обладают свойствами буферных растворов ( стр. Эти растворы почти нейтральны ( рН их находится в пределах от 6 до 8), и к ним можно прибавлять в известных пределах кислоты или щелочи без заметного изменения рН раствора. [15]
Страницы: 1 2