Свойство - скандий
Cтраница 1
Свойства скандия и иттрия весьма близки к свойствам лантана. Окиси скандия, иттрия и лантана соединяются с водой, образуя почти не растворимые в воде гидроокиси. Гидроокиси проявляют основной характер и взаимодействуют с кислотами, образуя соответствующие соли. [1]
Для изучении свойств скандия в распоряжении исследователей имелись лишь небольшие количества этого элемента, так что из-за отсутствия подробных сведений о нем в процессе многочисленных химических переработок его концентрировали вместе с редкоземельными элементами, поскольку он находится в 111 группе периодической таблицы. Это было вполне допустимо, но по мере того, как химические и физические свойства скандия становятся более известными, его нецелесообразно рассматривать вместе с редкоземельными элементами. Скандий является первым элементом переходной группы с одним Sd-электроном и обладает повышенной устойчивостью в металлическом состоянии, характерной для металлов с J-электронами. [2]
Так же интересны свойства треххлористого скандия. [3]
Свойства иттрия близки свойствам скандия, и для его фотометрического определения можно использовать те же хелатообразующие реагенты ( стр. Лантаноиды дают такие же реакции и мешают определению иттрия. [4]
Химические свойства иттрия подобны свойствам скандия и лантанидов. Подобно лантанидам, иттрий образует наиболее прочные комплексы с ли-гандами, содержащими кислород. [5]
Физические и химические свойства иттрия похожи на свойства скандия, лантана и тяжелых редкоземельных металлов, которым он сопутствует в минералах. [6]
Данные о механизме экстракции скандия довольно противоречивы. Наиболее достоверными и согласующимися со свойствами скандия ( и данными по экстракции других элементов, в частности РЗЭ), видимо, являются данные об экстракции его из азотнокислых растворов в виде сольвата Sc ( NO3) 3 - 3 ТБФ [2, 4, 5 ], хотя авторы работ [2, 6 ] считают возможным образование дисоль-вата Sc ( NO3) 3 - 2 ТБФ. [7]
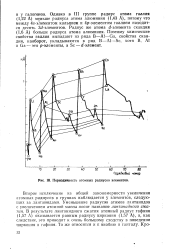 |
Периодичность атомных радиусов элементов. [8] |
Однако в III группе радиус атома галлия ( 1 22 А) меньше радиуса атома алюминия ( 1 43 А), потому что между 45-элементом кальцием и 4р - элементом галлием находится десять Sd-элементов. Поэтому химические свойства галлия выпадают из ряда В-Al - Ga, свойства скандия, наоборот, укладываются в ряд В - А1 - Sc, хотя В, А1 и Ga - это р-элементы, a Sc - - элемент. [9]
В этих словах выражено главное положение, под знаком которого Менделеев приводит все работы по периодическому закону начиная с 1875 г. К числу самых главных подтверждений этого закона, на опыте относятся следующие: во-первых, уже упоминавшиеся открытия предсказанных неизвестных ранее элементов и совпадение их свойств с тем, что было предугадано на основании периодического закона. В открытии галлия Лекок де - Буабодра-ном Менделеев сразу же увидел блестящее подтверждение периодического закона и вытекавших из него предвидений; это открытие нашло отклик у Менделеева ( ст. 11), а затем было обобщенно в изд. Нильсоном ( 1879 г.) и обнаружение в 1880 г., что свойства скандия совпадают с теми, которые были предсказаны для экабора, что также нашло у Менделеева отклик ( ст. 12), а затем было обобщено в изд. Винкле-ром ( 1886 г.) и совпадение его свойств со свойствами экасилиция, предсказанного Менделеевым. Это открытие было обобщено в изд. Is); отклик на него содержится в лекции 1886 г. ( см. доб. [10]
Самый легкий по атомному весу из редкоземельных элементов - скандий. Ко времени установления периодического закона он еще не был известен. Для него Д. И. Менделеевым было оставлено пустое место в IV периоде между кальцием и титаном под бором и алюминием; он был предварительно назван экабором. Этот элемент был открыт среди редкоземельных металлов скандинавским ученым Нильсоном и назван скандием. Сличая свойства скандия с предвычисленными Д. И. Менделеевым свойствами гипотетического экабора, Нильсон не замедлил убедиться, что скандий есть не что иное, как экабор. [11]
Ныне, когда этот элемент открыт проф. Винклером в Фрейберге ( в Саксонии), стало очевидно, что действительные его свойства вполне отвечают предугаданным, как это и выставил К. В этом должно видеть наглядное подтверждение справедливости периодического закона. Элемент этот ныне называется германием Ge ( см. гл. И не он один был предугадан периодическим законом. Мы увидим при описании элементов III группы, что свойства, подобным образом найденные для экваалюминия Е1 III - 5 ( около) 68, оправдались действительностью, когда Лекок-де - Боабодраном был найден металл, названный галлием. Точно также, по Ниль-сону, свойства скандия ответили свойствам экабора, предугаданные периодическою законностью. Отсюда уже видно, что периодический закон не только отвечает известной действительности, но и позволяет проникать хотя понемногу в неизвестную сущность химических элементов. Сведения о всяких действительно существующих предметах, а в том числе и о химических элементах, зародившись или возникнув и постоянно увеличиваясь, в сущности никогда не достигают конца, только всегда имеют возможность еще далее и более усовершенствоваться и пополняться. В этом ряде постепенного совершенствования достойно особого внимания и резко бросается в глаза накопление таких видов сведений, которые дают возможность предугадывать часть предметов, еще вовсе неизвестных, но действительно существующих. Очевидно, что при этом должна возрастать и вся доступная людям мера обладания предметами, подвергнутыми такой степени изучению. В той части химии, которая относится до элементов, предугадывание родилось с периодическим законом. А так как учение о химических элементах лежит в основах всех современных химических знаний, то явное усовершенствование в сведениях об элементах не могло не отразиться на многих частях нашей науки. Но за этой ступенью должны следовать еще многие и многие другие, поднятие на которые, так сказать, поощряется достигнутым успехом; границ здесь - при дружных трудовых усилиях многих адептов науки, рассеянных во всем мире, - полагать едва ли, на мой взгляд, возможно. [12]
Ныне, когда этот элемент открыт проф. Винклером в Фрейберге ( в Саксонии), стало очевидно, что действительные его свойства вполне отвечают предугаданным, как это и выставил К. В этом должно видеть наглядное подтверждение справедливости периодического закона. Элемент этот ныне называется германием Ge ( гл. И не он один был предугадан периодическим законом. Мы увидим при описании элементов III группы, что свойства, подобным образом найденные для экаалюминия EI - III - 5 ( около) 68, оправдались действительностью, когда Лекок де - Боабодраном был найден металл, названный галлием. Точно так же, по Нильсону, свойства скандия ответили свойствам экабора, предугаданные периодическою законностью. Отсюда уже видно, что периодический закон не только отвечает известной действительности, но и позволяет проникать хотя понемногу в неизвестную сущность химических элементов. Сведения о всяких действительно существующих предметах, а в том числе и о химических элементах, зародившись или возникнув и постоянно увеличиваясь, в сущности никогда не достигают конца, только всегда имеют возможность еще далее и более усовершенствоваться и пополняться. В этом ряде постепенного совершенствования достойно особого внимания и резко бросается в глаза накопление таких видов сведений, которые дают возможность предугадывать часть предметов, еще вовсе неизвестных, но действительно существующих. Очевидно, что при этом должна возрастать и вся доступная людям мера обладания предметами, подвергнутыми такой степени изучения. В той части химии, которая относится до элементов, предугадывание родилось с периодическим законом. А так как учение о химических элементах лежит в основах всех современных химических знаний, то явное усовершенствование в сведениях об элементах не могло не отразиться на многих частях нашей науки. Но за этой ступенью должны следовать еще многие и многие другие, поднятие на которые, так сказать, поощряется достигнутым успехом; границ здесь - при дружных трудовых усилиях многих адептов науки, рассеянных во всем мире, - полагать едва ли, на мой взгляд, возможно. [13]
Страницы: 1