Свойство - газовая смесь
Cтраница 2
Свойства идеальных растворов, подобно свойствам разреженных газовых смесей, не зависят от природы растворенного вещества, а определяются лишь их концентрацией. Следовательно, единственной причиной их образования ( как и образования газовых смесей) является возрастание энтропии при смешении. [16]
Свойства идеальных растворов, подобно свойствам разреженных газовых смесей, не зависят от природы растворенного вещества, а определяются лишь их концентрацией. [17]
Свойства идеальных растворов, подобно свойствам разреженных газовых смесей, не зависят от природы растворенного вещества, а определяются лишь его концентрацией. По некоторым свойствам к идеальным растворам близки бесконечно разбавленные растворы, в которых можно пренебречь взаимодействием частиц растворенного вещества из-за их разобщенности. [18]
Свойства идеальных растворов, подобно свойствам разреженных газовых смесей, не зависят от природы растворенного вещества, а определяются лишь их концентрацией. [19]
Свойства идеальных растворов, подобно свойствам разреженных газовых смесей, не зависят от природы растворенного вещества, а определяются лишь его концентрацией. По некоторым свойствам к идеальным растворам близки бесконечно разбавленные растворы, в которых можно пренебречь взаимодействием частиц растворенного вещества из-за их разобщенности. [20]
Возможности использования термодинамического подобия для исследования свойств газовых смесей значительно расширились благодаря работам Я. В этих работах показано, что в качестве опорных точек подобия может быть выбрана любая точка на поверхности состояния реального газа, отвечающая требованиям, предъявляемым к опорным точкам подобия. [21]
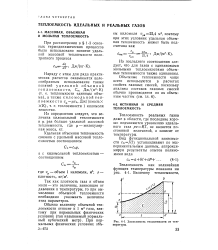 |
Зависимость теплоемкости от температуры. [22] |
Объемные теплоемкости чаще всего используются в расчетах свойств газовых смесей, поскольку анализы составов газовых смесей обычно производятся по их объемным частям ( см. гл. [23]
Эти модификации дают хорошие результаты по определению свойств газовых смесей, однако они не пригодны для описания поведения жидкой фазы, как углеводородной, так и неуглеводородной. [24]
Величина скорости распространения пламени зависит от физических параметров и свойств газовой смеси. Большое влияние на нормальную скорость горения оказывает температура газовой смеси. [25]
Величина v может быть определена исходя из данных о свойствах газовой смеси, таких, как вязкость, теплопроводность, диффузия, применяя для описания этих свойств рассматриваемую инверсионную модель. Для этой цели обычно используют температурную зависимость коэффициента вязкости. [26]
Хотя этот раздел относится к многокомпонентным системам, однако некоторые свойства газовых смесей целесообразно рассмотреть в настоящей главе, так как они непосредственно вытекают из свойств чистых газов. [27]
Другим широко используемым путем представления р - у / - свойств газовых смесей является закон аддитивности индивидуальных объемов Лмага. [28]
Другим широко используемым путем представления р - V - Г - свойств газовых смесей является закон аддитивности индивидуальных объемов Амага. [29]
В основе работы любого анализатора молекулярных микрокомпонентов атмосферы лежит зависимость между каким-либо свойством газовой смеси и концентрациями веществ, входящих в ее состав. [30]
Страницы: 1 2 3