Свойство - однотипное соединение
Cтраница 1
Свойства однотипных соединений по группе закономерно изменяются. Например, основные свойства оксидов ( ЭО) и гидроксидов ( Э ( ОН) 2) от цинка к ртути усиливаются. [1]
Различия в свойствах однотипных соединений фосфора и азота объясняются различием в эффективных размерах валентных s - и р-орбиталей атомов. [2]
Согласно другой точке зрения отличия свойств однотипных соединений фосфора и азота объясняются наличием у фосфора вакантных d - орбиталей В последнее время справедливость такого объяснения подвергается сомнению. [3]
Сущность ее заключается в зигзагообразном изменении некоторых свойств однотипных соединений при переходе элементов сверху вниз по группам периодической системы. Наблюдается вторичная периодичность сравнительно редко, наиболее отчетливо она проявляется при характеристичных валентностях сопоставляемых элементов и в тех случаях, когда к членам малых периодов присоединяют для совместного рассмотрения элементы правых подгрупп. [4]
Сущность ее заключается в зигзагообразном изменении некоторых свойств однотипных соединений при переходе элементов сверху вниз по группам периодической системы. [5]
Для отделения скандия от сопутствующих ему элементов предложено большое количество методов, в которых используются весьма незначительные различия в свойствах однотипных соединений. До настоящего времени большинство предложенных методов было реализовано в лабораторных масштабах, поэтому часто их даже трудно отделить от аналитических. [6]
Способность некоторых РЗЭ переходить из одной степени окисления в другую используется в технологии разделения, так как в этом случае проявляется гораздо большая разница в свойствах однотипных соединений. [7]
Наконец, следует учитывать [129], что элементы второго ряда периодической системы ( в меньшей степени - третьего ряда) в состоянии положительной валентности иногда обнаруживают меньшую аналогию в свойствах однотипных соединений, чем элементы из той же подгруппы с большими атомными весами. Это связано с тем, что катионы этих элементов обладают более существенными отличиями электронных оболочек и соответственно размеров и потенциалов ионизации. В области высоких температур ( выше 2000 - 3000 К) систематические отклонения наблюдаются иногда для соединений более тяжелых элементов, что свидетельствует, по-видимому, о влиянии возбуждения новых энергетических уровней и усилении ангармоничности колебаний атомов в молекулах. [8]
Способность Се3, Рг3 и ТЬ3 окисляться до четырехвалентного состояния, a Sm3, Eu3 и Yb3 восстанавливаться до двухвалентного ( соответствующие значения электродных потенциалов приведены в табл. 37) используется для выделения их из смеси с остальными РЗЭ, так как в этом случае проявляется гораздо большая разница в свойствах однотипных соединений. [9]
Наибольшей сложностью отличается фракционированная кристаллизация солей рубидия, при которой в зависимости от порядка изменения растворимости соединений в ряду щелочных металлов в твердой фазе накапливаются примеси либо калия, либо цезия. Обычно свойства однотипных соединений калия, рубидия и цезия закономерно изменяются в направлении увеличения порядкового номера элемента. Это наряду с высокой растворимостью почти исключает возможность применения простых солей для разделения трех близких по свойствам щелочных элементов. [10]
Близость химических свойств переходных элементов определяет и близость свойств их однотипных соединений. Наибольшей близостью характеризуются свойства простых однотипных соединений в степени окисления элемента 2 и 3, образованных при участии двух s - электронов и одного d - электрона. Для тяжелые d - элементов такие соединения нехарактерны. [11]
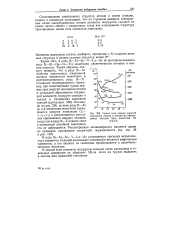 |
Сумма трех первых энергий ионизации атомов и энтальпии образования оксидов Э2О3 элементов III группы. [12] |
Кроме того, в ряду В-Al - Sc-Y-La - Ас ( в противоположность ряду В-Al - Ga-In-Tl) монотонно увеличиваются атомные и ионные радиусы. Таким образом, следует ожидать, что в ряду В-Ас свойства однотипных соединений должны изменяться монотонно в противоположность ряду В-Tl. Как видно из рис. 238, во всем ряду В-Ас ( р - и d - элементов) монотонно уменьшаются энергии ионизации ( / х 2 / з) и увеличиваются энтальпии образования высших оксидов, тогда как в ряду В-Tl ( одних лишь р-элементов) подобной монотонности не наблюдается. Рассмотренная закономерность является одним из примеров проявления вторичной периодичности ( см. стр. [13]
Поэтому кремний - элемент 3-го периода - по структуре и свойствам однотипных соединений существенно отличается от углерода - элемента 2-го периода. Максимальное координационное число кремния равно шести, а наиболее характерное - четырем. Как и для других элементов 3-го периода, рл, - рл - связывание для кремния не характерно и потому в отличие от углерода sp - и s / 72-гибридные состояния для него неустойчивы. [14]
 |
Энергия связей. [15] |
Страницы: 1 2