Общее химическое свойство
Cтраница 1
 |
Реакции, лежащие в основе получения металлов. [1] |
Общее химическое свойство металлических s - и р-эле-ментов - это их способность легко отдавать валентные электроны вследствие гораздо большего атомного радиуса по сравнению с неметаллическими элементами. Поэтому образованные ими простые вещества в химических реакциях выполняют функцию восстановителей. [2]
Общие химические свойства кремния и основанные на них аналитические реакции находятся в связи с положением его в четвертой группе системы Менделеева, на четвертом месте от предшествующего ему и от следующего за ним инертного газа. [3]
Общие химические свойства кремния и германия определяются положением этих элементов в таблице Менделеева. Кремний и германий находятся в четвертой группе таблицы, располагаясь соответственно в третьем и четвертом периодах. Во всех своих соединениях кремний и германий выступают как четырех - или двухвалентные элементы. При умеренных температурах ( до 700 К) и в особенности во влажных средах они образуют, как правило, четырехвалентные соединения. Наоборот, при высоких температурах ( порядка 1300 К) и в сухой атмосфере более типичными являются двухвалентные соединения рассматриваемых элементов. Химические связи в соединениях кремния и германия с элементами крайних групп таблицы Менделеева - полярные и обладают существенным дипольным моментом. Типичным для таких соединений является их взаимодействие с полярными молекулами других веществ и, в первую очередь, с молекулами воды. Соединения с чисто ионной связью для кремния и германия не известны. Следует, однако, иметь в виду, что некоторые полярные соединения рассматриваемых элементов могут частично диссоциировать на соответствующие положительные и отрицательные ионы. [4]
 |
Удельные веса металлов весом 053. таким образом, са. [5] |
Прочие общие химические свойства металлов, которые пр-иходится указывать да ранней ступени обучения химии-способность замешать в кислотах водород, основной характер гидратов окислов, являются лишь следствиями указанного основного общего свойства металлов. [6]
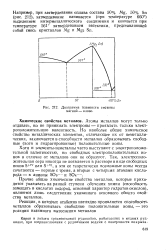 |
Диаграмма плавкости системы магний - олово. [7] |
Прочие общие химические свойства металлов, которые приходится указывать на ранней ступени обучения химии ( способность замещать в кислотах водород, основной характер гидратов окислов), являются лишь следствиями указанного основного общего свойства металлов. [8]
Общие химические свойства транскалифорниевых элементов группы актинидов были предсказаны Сиборгом [ S92 ] на основании гипотезы об актинидах и аналогий с группой редкоземельных переходных элементов. [9]
Общим химическим свойством спиртов и фенолов является образование простых и сложных эфиров. [10]
Общими химическими свойствами спиртов и фенолов является образование простых и сложных эфиров. [11]
Общим химическим свойством металлов является их относительно высокая восстановительная способность. Восстановительные свойства металлов ослабляются в ряду активности слева направо. [12]
Общими химическими свойствами элементов будем называть такие свойства, которые проявляются ими во многих соединениях и являются обычными, типичными для них. [13]
Общим химическим свойством спиртов и фенолов является образование простых и сложных эфиров. [14]
Основным общим химическим свойством металлов является то, что они сравнительно легко отдают валентные электроны и переходят в положительно заряженные ионы. Способность атома отдавать свои валентные электроны называют его восстановительными свойствами. Металлы обладают сильными восстановительными свойствами. С увеличением металлических свойств усиливаются восстановительные свойства. [15]
Страницы: 1 2 3