Равновесное свойство
Cтраница 1
Равновесные свойства определяются состоянием - как исходных веществ, так и продуктов реакции. Для термодинамики важны левая и правая части химического уравнения. Скорость реакции определяется только состоянием исходных веществ. Для кинетики важна только левая часть уравнения реакции. [1]
Равновесные свойства рассматриваемой ДС, очевидно, определяются энергией иш и доменных границ. [2]
Равновесные свойства растворов относятся к раствору как к целому и могут быть весьма разнообразны вследствие взаимодействия между молекулами ( или атомами) компонентов раствора. Ввиду этого разнообразия в поведении растворов необходимо ввести их классификацию. Термодинамическая классификация растворов, основана на характере уравнений для химических потенциалов компонентов раствора. [3]
Равновесные свойства молекул представляют результат усреднения по свойствам поворотных изомеров. [4]
Равновесные свойства газа оказываются особенно простыми, когда занимаемый им объем очень велик и очень велика его энергия. [5]
Равновесные свойства ДС определяются размером и формой образцов, ориентацией их поверхностей по отношению к ОЛН, а также количеством ОЛН, которыми может обладать ферромагнетик. [6]
Равновесные свойства электрохимических цепей, а также закономерности протекания через них электрического тока являются предметом электрохимической науки. Существенные элементы электрохимической цепи - металлические ( или полупроводниковые) электроды, проводники второго рода ( растворы электролитов, их расплавы или твердые электролиты) и границы раздела фаз между металлом ( полупроводником) и электролитом, между двумя различными проводниками 1-го рода и между двумя различными электролитами. [7]
Равновесные свойства неидеальных растворов определяют термодинамическим путем при помощи эмпирического метода активности, предложенного Льюисом. [8]
Равновесные свойства идеальной системы, представляют собой предельные свойства определенных реальных систем при некоторых четко оговоренных условиях, рассматриваемых в гл. [9]
Равновесные свойства идеальных систем относятся к наиболее традиционным вопросам статистической механики. Они рассмотрены во всех общих руководствах, цитированных в гл. [10]
Эти равновесные свойства с течением времени претерпевают небольшие колебания около средних значений - флуктуации. [11]
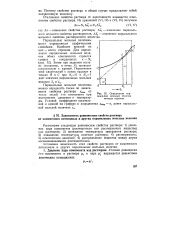 |
Определение парциальных мольных величин методом отрезков. [12] |
Рассмотрим следующие равновесные свойства раствора: 1) давление пара компонента ( растворителя или растворенного вещества) над раствором; 2) понижение температуры замерзания раствора; 3) повышение температуры кипения раствора; 4) растворимость; 5) осмотическое давление; 6) распределение вещества между двумя несмешивающимися растворителями. [13]
 |
Потенциал межатомного взаимодействия Е ( г в зависимости от межъядерного расстояния г. Горизонтальными линиями отмечены уровни энергии атома с учетом энергии. [14] |
Многие равновесные свойства твердых тел, в том числе и структурные, определяются в значительной мере, а в ряде случаев и полностью, ангар-монизмом потенциала взаимодействия атомов. Именно энгармонизм, наряду с колебаниями атомов ( в том числе нулевыми), приводит к изотопическому эффекту в постоянной кристаллической решетки твердого тела. Потенциал взаимодействия Е ( г ] двух атомов в твердом теле представлен схематично на рис. 12.1.1. В первом приближении равновесное расстояние г между ближайшими соседями и, соответственно, постоянная решетки определяются минимумом потенциала взаимодействия. Отметим, что потенциал не зависит от температуры и массы взаимодействующих частиц. Различие между изотопами оказывается наибольшим при низких температурах и уменьшается с ростом температуры. [15]
Страницы: 1 2 3 4