Равновесное свойство - система
Cтраница 1
Равновесные свойства системы имеют очень важное значение. Выбор абсорбента, растворителя или адсорбента является решающим фактором. Обычно требуется обработать поток с целью удаления примесей или извлечения ценного продукта. [1]
При выборе параметров в варианте 1 потенциалом термодинамическим, содержащим в себе всю информацию о равновесных свойствах системы, является энтропия S S (, V, N, А), в варианте 2 - свободная энергия ( Ге. [2]
Необходимо обратить внимание на важность совместной формулировки и решения как прямых, так и обратных задач с целью получения обобщающей обработки данных о всех равновесных свойствах интересующей системы, включая и термодинамические функции фаз и условия их равновесия. Пока такое единство достигнуто лишь в отдельных частных примерах. Как правило же, исследовательские лаборатории, занимающиеся соответствующими проблемами, существуют раздельно и работают независимо друг от друга, а справочные издания содержат диаграммы состояния и термодинамические функции веществ, взаимно не согласованные между собой. [3]
Равновесные свойства системы в значительной степени определятся тем, каково различие между энергиями взаимодействия пар типа А - А, В - В и А - В. [4]
Равновесные свойства системы в значительной степени определяется тем, каково различие между энергиями взаимодействия пар типа А-А, В-В и А-В. [5]
Дисперсность ( или удельная поверхность) является самостоятельным термодинамическим параметром состояния системы, изменение которого вызывает соответствующие изменения других равновесных свойств системы. Наглядным примером влияния дисперсности на равновесные свойства системы может служить распределение ПАВ в гетерогенной системе вода - бензол. ПАВ концентрируется на поверхности раздела фаз. Если эта система находится в высоком узком цилиндре, то межфазная поверхность будет небольшая, п количество адсорбированного па ней ПАВ будет также мало. Если содержимое из цилиндра нсфелпть в противень, межфазпая поверхность значительно возрастает. Общее количество ПАВ на поверхности увеличится, а концентрация его в объемах фаз соответственно уменьшится. [6]
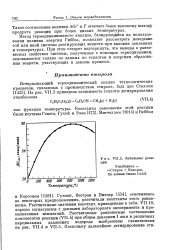 |
Энтальпия реакции. [7] |
Метод термодинамического анализа, базирующийся на использовании величин энергии Гиббса, позволяет рассмотреть поведение той или иной системы реагирующих веществ при высоких давлениях и температурах. При этом следует подчеркнуть, что выводы о равновесных свойствах системы, полученные с помощью термодинамики, основываются только на данных по теплотам и энергиям образования веществ, участвующих в данном процессе. [8]
Для такого рассмотрения необходимо задать модель кристаллической решетки и способ выражения энергии кристалла через параметры, имеющие смысл энергий элементарных взаимодействий в кристалле. Это позволяет сконструировать явное выражение для статистической суммы и, применив условие равновесия, получить равновесные свойства системы и значения параметров. Основоположники теории кристаллов с дефектами, Вагнер и Шотки [53, 54], применили приближение аддитивных вкладов в термодинамические функции кристаллов от всех сортов дефектов, выразили конфигурационную энтропию через число дефектов каждого сорта и, использовав условия равновесия кристалла, получил зависимости активностей компонентов от величины от клонения от рационального стехиометрического состава для конкретных случаев наличия тех или иных комбинаций дефектов. [9]
Для этого рассмотрения необходимо задать модель кристаллической решетки и выразить энергию кристалла через параметры, имеющие смысл энергий элементарных взаимодействий в кристалле. Это позволяет сконструировать явное выражение для статистической суммы и, применив условие равновесия, получить равновесные свойства системы и значения параметров. [10]
Благодаря такому свойству свободной энергии статистическая сумма играет важнейшую роль в равновесной статистической механике. Нам не приходится рассчитывать каждую новую термодинамическую функцию по отдельности, ибо Z ( Т, 37, N) заключает в себе всю информацию о термодинамически равновесных свойствах системы. В этом смысле можно утверждать, что проблема равновесной термодинамики в принципе полностью решена. Разумеется, расчет статистической суммы в явном виде - совсем не простая задача; в общем случае он связан со значительными математическими трудностями. Однако трудности эти носят скорее технический, нежели принципиальный характер, поскольку в каждом случае известно, что мы хотим вычислить. [11]
Описанная процедура полностью аналогична конечно-разностной схеме при решении численными методами задач математической физики. Однако принципиальное отличие послойной модели заключается в том, что приближение послойного решения к детерминированному ( о способе приближения см. далее) происходит не в случае Да; - vO, Ai - 0, как в сходящихся численных методах, а в случае, когда объем элементарного слоя т и объем элементарной порции V равны некоторым конечным значениям ( т, V), определяемым кинетическими и равновесными свойствами системы. [12]
В этом разделе обсуждается влияние некоторых факторов, которое можно экспериментально установить и контролировать, на системы, находящиеся в состоянии равновесия. Качественные предсказания влияния различных переменных величин могут быть сделаны на основании принципа Ле-Шателье, который гласит, что если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то положение равновесия сместится в направлении, уменьшающем или ослабляющем это воздействие. Количественные изменения в равновесных свойствах системы, вызванные, например, изменениями давления или температуры, можно оценить, исходя из выражения для константы равновесия или из других термодинамических соотношений. [13]
Проблемой исследования свойств макроскопических систем, находящихся в состоянии равновесия, на основании известных свойств образующих такие системы частиц занимается статистическая физика. Основная задача заключается в том, чтобы описать поведение системы, содержащей весьма большое число частиц ( например, 1 кг или 1 кмоль реального газа), по свойствам и законам движения отдельных молекул, которые считаются заданными. Поведение макроскопических систем определяется закономерностями особого рода - статистическими закономерностями. Общие равновесные свойства системы ( например, термодинамические параметры, характеризующие ее состояние) сравнительно мало зависят от конкретных свойств частиц и законов их взаимодействия. Следует отметить, что последовательное применение статистических методов нельзя осуществить на основе классической механики движения частиц. Даже для описания движения сравнительно тяжелых частиц ( молекул) в объеме макроскопической системы, когда, казалось бы, справедливы положения ньютоновской механики, приходится использовать теорию движения микрочастиц - квантовую механику. Таким образом, получение уравнения состояния реальных газов теоретическим путем в принципе возможно, но для большинства практически важных случаев связано с непреодолимыми трудностями. Однако теория позволяет обосновать общий вид уравнения состояния. [14]
Страницы: 1