Индивидуальное свойство - вещество
Cтраница 2
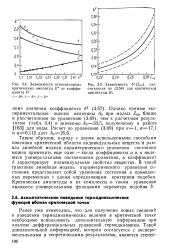 |
Зависимости относительных [ IMAGE ] Зависимость 62 ( ZKP, pac. [16] |
Тайим образом, наряду с двумя используемыми способами описания критической области индивидуальных веществ в рамках линейной модели параметрического уравнения состояния можно применить еще один - когда коэффициенты а и к являются универсальными постоянными уравнения, а коэффициент b характеризует индивидуальные свойства вещества. В такой трактовке линейная модель параметрического уравнения состояния представляет собой уравнение состояния в приведенных переменных с одним определяющим критерием подобия. [17]
Твердое состояние возникает в том случае, когда повышается энергия взаимодействия молекул, приводящая к осуществлению в твердом теле лишь колебательных движений молекул или ионов около фиксированного в пространстве положения равновесия. В твердом теле отсутствует текучесть и в значительной степени проявляются индивидуальные свойства вещества. Твердые тела имеют свою собственную устойчивую форму и сохраняют свой объем, проявляя большое сопротивление к изменению формы и объема при воздействии внешних сил. [18]
Газообразное состояние возникает тогда, когда энергия теплового движения молекул вещества превышает энергию их взаимодействия. Молекулы вещества в этом состоянии приобретают прямолинейное поступательное движение, а индивидуальные свойства веществ теряются, и они подчиняются общим для всех газов законам Газообразные тела не имеют собственной формы и легко изменяют свой объем при воздействии внешних сил или при изменении температуры. [19]
Взрывчатые соединения могут получаться в качестве промежуточных продуктов при синтезах и как побочные, иногда случайные вещества при других работах. Приводимые ниже отдельные примеры имеют целью показать разнообразие взрывчатых веществ и условий их получения, а также подтвердить общее положение о необходимости тщательно знакомиться по специальным руководствам с особыми, индивидуальными свойствами веществ и смесей, которые будут использованы или могут получиться при выполнении работ. [20]
В мощных ударных волнах происходят интенсивные сжатие и нагрев вещества и тем самым создается уникальная возможность исследований его фундаментальных свойств в экстремальных условиях. Сжимаемость среды под действием давления и зависимость ее плотности от температуры или энергосодержания описываются уравнениями состояния. Уравнение состояния выражает индивидуальные свойства вещества и необходимо для любых расчетов высокоэнергетических процессов в сплошной среде. По этой причине проблема широкодиапазонных уравнений состояния явилась стимулом для становления и развития физики ударных волн и до сего времени остается одним из основных направлений исследований. При решении многих современных задач возникает необходимость рассчитывать состояния вещества, находящегося в разных своих точках как в конденсированной, так и в газовой фазах одновременно. Возникает необходимость объединения теоретических представлений и экспериментальных данных для различных фазовых состояний. [21]
Различные газы ( воздух, азот, кислород, неон, водород, гелий и др.) и их смеси являются наиболее распространенными рабочими телами низкотемпературных установок. Молекулы газов находятся в непрерывном движении. Силы взаимодействия между ними определяются индивидуальными свойствами вещества, строением ко-лекул и значениями давления и температуры. Известно, что интенсивность молекулярного движения обусловливает определеннее значение температуры и кинетической энергии, а сила межмолекулярного сцепления определяет агрегатное состояние вещества и потенциальную энергию. Несмотря на то, что молекулы газов движутся с большими скоростями, силы взаимного притяжения могут быть весьма значительными и с ними необходимо считаться. Кроме того, при определенных условиях ( большие давления и плотности) на свойства газа влияют размеры молекул. При этих же условиях можно пренебречь размерами молекул, так как они значительно меньше расстояний между ними. [22]
Различные газы ( воздух, азот, кислород, неон, водород, гелий и др.) п их смеси являются наиболее распространенными рабочими телами низкотемпературных установок. Молекулы газов находятся в непрерывном движении. Силы взаимодействия между ними определяются индивидуальными свойствами вещества, строением молекул и значениями давления и температуры. Известно, что интенсивность молекулярного движения обусловливает определеннее значение температуры и кинетической энергии, а сила межмолекулярного сцепления определяет агрегатное состояние вещества и потенциальную энергию. Несмотря на то, что молекулы газов движутся с большими скоростями, силы взаимного притяжения могут быть весьма значительными и с ними необходимо считаться. Кроме того, при определенных условиях ( большие давления и плотности) на свойства газа влияют размеры молекул. При этих же условиях можно пренебречь размерами молекул, так как они значительно меньше расстояний между ними. [23]
Соотношение (3.34) раскрывает физический смысл постоянной Рао и ее некоторые свойства. В соотношение (3.34), кроме универсального постоянного множителя В, входят только величины 1 / кр, Ткр и М, характеризующие индивидуальные свойства вещества. Как можно видеть из (3.34), определяющее значение в этом случае имеет молярный критический объем. [24]
Влияние вакуума, как указывалось, идентично присутствию водяного пара. Штаге [28], изучая разделение высших жирных кислот, указывает, что в случае использования вакуума разделяемость компонентов лучше, чем при использовании водяного пара. Данные других авторов [29], наоборот, показывают, что в случае использования водяного пара разделяемость смесей уменьшается. Очевидно на нее оказывают влияние индивидуальные свойства веществ. [25]
Страницы: 1 2