Магнитное свойство - атом
Cтраница 4
 |
Разрешенные энергетические состояния электронов в атомах по периодам. [46] |
После f названия идут уже по алфавиту. В принципе, главного и побочного числа было бы достаточно для обозначения всех возможных энергетических состояний, если бы не магнитные свойства атома и электрона. [47]
Нам представлялось, что наряду с этими монографиями желательно предоставить в распоряжение студентов 3 - 4 курсов небольшой учебник, в котором были бы собраны основные теоретические и экспериментальные сведения по ферромагнетизму. Так как отчетливое понимание сущности ферромагнитных явлений возможно только при предварительном знакомстве с общим учением о магнетизме, первые шесть глав отведены магнитным свойствам атомов и пара - и диамагнетизму. Остальная часть книги посвящена ферромагнетизму. В 7 - 9 главах даны основы теории самопроизвольной намагниченности. В 10 - 14 главах рассматривается теория технической кривой намагничивания и в последней-15 - й - описываются основные ферромагнитные материалы. [48]
Обычно насыщение можно наблюдать только при очень низких температурах. В системе магнитных атомов, далеко отстоящих друг от друга, парамагнитная восприимчивость может служить мерой магнитных моментов отдельных носителей и давать информацию о магнитных свойствах атомов, составляющих систему. Однако в твердых телах, содержащих много парамагнитных атомов или ионов, обычно имеют место взаимодействия магнитных электронов с магнитными или электростатическими полями соседних атомов. Эти воздействия нарушают идеальное поведение магнитных носителей, и хотя в твердых телах наблюдаются магнитные эффекты той же природы, что и в системе рассредоточенных магнитных атомов, эти эффекты уже нельзя использовать для получения простой информации о числе магнитных электронов на атом. Таким образом, парамагнитная восприимчивость, давая в общем полезную информацию о веществе, непосредственно не связана с факторами, важными с точки зрения металлургии и определяющими структуру материала. [49]
Наряду со слабомагнитными телами существует ряд веществ, например ферромагнетики, для которых намагниченность не является линейной функцией поля. Для диамагнетиков характерно, что восприимчивость, как правило, не зависит от температуры, а для парамагнетиков она часто изменяется обратно пропорционально абсолютной температуре. Магнитные свойства атома обусловлены следующими факторами: орбитальным движением электронов; спиновыми эффектами; магнетизмом атомного ядра; Нейтроны и протоны, составляющие ядро, обладают собственными магнитными моментами. Однако величина магнитного момента нуклона из-за того, что его масса почти в 2000 раз больше массы электрона, пренебрежимо мала по сравнению с магнитным моментом электрона. Вычисление суммарных моментов атомов облегчается тем, что как суммарный орбитальный, так и суммарный спиновый момент полностью застроенных электронных оболочек равен нулю. Поэтому следует принимать во внимание лишь электроны, занимающие незаполненные оболочки. [50]
Итак, в атоме железа спины четырех электронов в третьем слое остаются некомпенсированными. Что касается наружных валентных электронов атома железа, то их спины, вообще говоря, тоже могут быть некомпенсированы. Однако, как показывает опыт, на магнитные свойства атома железа валентные электроны, слабо связанные с атомом, существенного влияния не оказывают. [51]
Временный выход из положения был найден при помощи введения гипотезы о вращающемся электроне, которая в свою очередь приводила к новым противоречиям и затруднениям. После нахождения уравнения Шредингера выяснилось, однако, что квантовая механика в шредингеровской форме также бессильна дать правильный ответ на вопрос о магнитных свойствах атома водорода. [52]
Магнитную активность проявляют все вещества без исключения, поэтому естественно предположить, что магнитные свойства вещества определяются элементарными частицами, входящими в состав каждого атома. Такими одинаковыми для всех атомов частицами являются электроны, протоны и нейтроны. Исследования показали, что магнитные моменты протона и нейтрона почти на три порядка ниже наименьшего магнитного момента электрона, поэтому в первом приближении можно пренебречь магнитным моментом ядра, состоящего из протонов и нейтронов, и полагать, что магнитные свойства атома целиком определяются электронами. Это положение является фундаментальным в электронной теории магнетизма, которая общепринята в учении о магнетизме. [53]
Наконец, несмотря на усовершенствования, внесенные в теорию Бора другими учеными ( была принята во внимание возможность движения электрона в атоме не только по круговым, но и по эллиптическим орбитам, по-разному расположенным в пространстве), эта теория не смогла объяснить некоторых важных спектральных характеристик многоэлектронных атомов и даже атома водорода. Например, оставалась неясной причина различной интенсивности линий в атомном спектре водорода; не объяснялась тонкая структура спектров атомов, заключающаяся в том, что их отдельные линии расщепляются на несколько других. Сами количественные расчеты многоэлектронных атомов оказались чрезвычайно сложными и практически неосуществимыми. Теория ошибочно описывала магнитные свойства атома водорода, принципиально не могла объяснить образование химической связи в молекулах. [54]
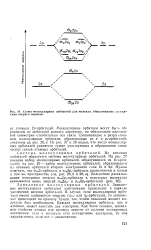 |
Схема молекулярных орбиталей для молекул, образованных элементами второго периода. [55] |
Заполнение молекулярных орбиталей электронами происходит в порядке увеличения энергии орбиталей. В случае, если молекулярные орбп-тали имеют одинаковую энергию ( ясв - или Яр-орбитали), то заполнение происходит по правилу Хунда, так, чтобы спиновый момент молекулы был наибольшим. Каждая молекулярная орбиталь, как и атомная, может вместить два электрона. Как было сказано, магнитные свойства атомов или молекул зависят от наличия неспаренных электронов: если в молекуле есть неспаренные электроны, то она парамагнитна, если нет - диамагнитна. [56]
Атомы всех веществ содержат движущиеся элементарные частицы, несущие электрические заряды, так, электроны атомов движутся вокруг их ядер и вращаются вокруг своих осей. Каждая движущаяся заряженная частица обладает магнитным моментом. Таким образом, атом любого вещества представляет сложную магнитную систему, Магнитный момент атома определяется векторной суммой магнитных моментов отдельных образующих его частиц. Магнитные моменты протонов и нейтронов примерно в 1000 раз меньше магнитных моментов электронов, поэтому полагают, что магнитные свойства атома определяются в основном орбитальными и спиновыми магнитными моментами его электронной оболочки. Взаимная ориентация спиновых и орбитальных магнитных моментов различна в атомах различных веществ, поэтому различны также и их магнитные свойства. [57]
Электроны в атоме стремятся занять места в оболочках и подоболочках, ближе расположенных к ядру, так как энергия электрона при этом уменьшается и его состояние делается более устойчивым. Вопрос о том, как в соответствии с принципом Паули происходит заполнение электронами оболочек и подоболочек, подробно рассмотрен в третьем томе курса. Сейчас обратим внимание лишь на одну особенность ферромагнитных металлов. В этих атомах нарушается последовательность заполнения электронами мест в ойо-лочках и слоях. Прежде чем полностью застроится нижняя оболочка, начинается заполнение выше расположенной оболочки. Поэтому в переходном атоме появляются не заполненные электронами внутренние слои и оболочки. Например, в атоме железа 26 его электронов распределены на четырех оболочках. Первая и вторая оболочки целиком заполнены и содержат соответственно 2 и 8 электронов. Спины электронов, расположенных в каждом слое, могут быть ориентированы в двух противоположных направлениях. В застроенных первых двух оболочках атома железа магнитные спиновые моменты электронов взаимно компенсируют друг друга. В третьей оболочке первые два слоя также характерны тем, что спиновые магнитные моменты электронов, расположенных в этих слоях, компенсируют друг друга. Что же касается третьего слоя, то из шести находящихся в нем электронов пять имеют спины, ориентированные в одном направлении1, и лишь один электрон имеет спин, ориентированный противоположно. Итак, в атоме железа четыре электронных спина в третьей оболочке остаются некомпенсированными. Что касается наружных валентных электронов атома железа, то их спины, вообще говоря, тоже могут быть некомпенсированы. Однако, как показывает опыт, на магнитные свойства атома железа валентные электроны, слабо связанные с атомом, существенного влияния не оказывают. [58]
Страницы: 1 2 3 4