Основное свойство - соединение
Cтраница 1
Основные свойства соединений возрастают от германия к свинцу а кислотные свойства уменьшаются в обратном порядке. [1]
Основные свойства соединений этого элемента, относящегося к основной Подгруппе главной группы, напоминают соответствующие Свойства соединений сурьмы. В этом состоянии окисления он известен лишь в виде виамутатов металлов. [2]
Ниже приведены таблицы, содержащие основные свойства соединений, описанных в этой статье. В таблицы включены только такие соединения, в действительном получении и идентификации которых имеется полная уверенность. Смеси изомеров в таблицы не включались, если не считать случаев, когда вещество представляет особый интерес. Список литературы не является исчерпывающим; он ограничивается ссылками на работы, в которых приведены описываемые свойства. [3]
Кроме того, этот образ характеризуется определенными основными свойствами соединения и характеристиками самого процесса измерения. [4]
При замещении водородных атомов аммиака жирными радикалами основные свойства соединения усиливаются; наивысшей основностью обладают четвертичные аммониевые основания. Гидрат окиси тетраметиламмония является почти таким же сильным основанием, как едкий натр. [5]
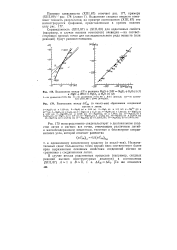 |
Взаимосвязь между Л5 в реакциях MgO 2HF MgF2 Н20 ( г ( / и MgO 2HC1 MgCl2 Н2О ( г ( 2.| Взаимосвязь между AG29g ( в ккал / г-экв образования соединений. [6] |
Незначительный сдвиг большинства точек вправо вниз соответствует более ярко выраженным основным свойствам соединений магния по сравнению с соединениями лития. [7]
 |
Электропроводность растворов некоторых соединений. [8] |
Основные свойства нитросоединений и сульфонов выражены значительно слабее, чем основные свойства соединений, содержащих только один атом кислорода с двойной связью. [9]
Особенностью ауксохромов является то, что все они обусловливают кислотные или основные свойства соединения и выполняют еще одну важную функцию - способствуют взаимодействию органического соединения с окрашиваемым материалом. В молекуле красителя может присутствовать несколько различных по природе ауксохромных группировок. Если у красителя преобладают основные свойства, то он называется основным красителем, а если кислотные, - то кислотным. Существуют и нейтральные красители. [10]
Большинство протонсодержащих соединений включает в себя гетероатомы с неподеленной парой электронов, поэтому говорить о кислотных или основных свойствах соединений имеет смысл лишь по отношению к какому-либо другому веществу, когда эти свойства проявляются в конкретной реакции - кислотно-основном равновесии. [11]
Не говоря о существующих различиях в физических свойствах ( температура плавления и кипения, плотность металлов и их пяти-окисей), в числе особо важных химических отличий ниобия и тантала необходимо указать прежде всего на более основные свойства соединений тантала по сравнению с соединениями ниобия. Это отличие ведет к практически важной большей способности некоторых соединений ниобия гидролизоваться в сравнении с аналогичными по составу соединениями тантала. На этом основаны наиболее важные способы разделения ниобия и тантала. [12]
Для выделения ядов из высушенных шкурок жаб шкурки выдерживают в течение нескольких месяцев в разбавленном спирте, выпаривают растворитель в вакууме и обрабатывают затем остаток водой, причем генин и буфотоксин выладают в осадок, а обладающие основными свойствами соединения переходят в раствор в виде солей. Из одной высушенной шкурки весом около 15 г получается 7 - 10 мг генина. [13]
Вещества, совмещающие в себе свойства кислот и оснований, называются амфотерными. Основные свойства амфотер-ных соединений проявляются в кислой среде, а кислотные - в щелочной. Амфотерными соединениями являются А1 ( ОН) 3, Zn ( OH) 2, Pb ( OH) 2, белки, пептиды, аминокислоты и др. Кислотные и основные свойства амфотерных гидроокисей слабы, поэтому они проявляются в сияьнокислой и сильнощелочной среде. [14]
Цинк - активный металл, легко растворяется в кислотах, его соединения слабо амфотерны. При переходе к ртути основные свойства соединений несколько усиливаются, но химическая активность свободного металла резко падает. Ртуть интересна тем, что является единственным жидким металлом при нормальных условиях, встречается в самородном виде. Пары кадмия и ртути очень ядовиты. [15]
Страницы: 1 2