Кинетическое свойство - система
Cтраница 1
Кинетические свойства системы обусловлены подвижностью молекул или атомов. В растворах полимеров присутствуют большие макромолекулы, время релаксации которым очень велико. Поэтому все процессы в истинных растворах полимеров происходят очень медленно, что делает их похожими на коллоидные системы. Но в отличие от коллоидная систем, малая скорость процессов, происходящих в истинных растворах полимеров, не евя зана с перавновее-ностью системы. Истинные растворы полимеров - это термодина мически устойчивые равновесные системы. Состояние равновесия устанавливается в них очень медленно вследствие очень больших времен релаксации цепных молекул, причем время релаксации тем больше, чем выше концентрация полимера в растворе. Рассмотрим это явление подробнее. [1]
 |
Диаграмма состояния си - а полимер в ней отсутствует. [2] |
Кинетические свойства системы обусловлены подвижностью молекул или атомов. В растворах полимеров присутствуют большие макромолекулы, время релаксации которых очень велико. [3]
Кинетические свойства системы обусловлены подвижностью молекул или атомов. В растворах полимеров присутствуют большие макромолекулы, нремя релаксации которых очень велико. Поэтому все процессы в истинных растворах полимеров происходят очень медленно, что делает их похожими на коллоидные системы. Но в отличие от коллоидных систем, малая скорость процессов, происходящих в истинных растворах полимеров, не связана с неравновесностью системы. Истинные растворы полимеров - это термодинамически устойчивые равновесные системы. Состояние равновесия устанавливается в них очень медленно вследствие очень больших времен релаксации цепных молекул, причем время релаксации тем больше, чем выше концентрация полимера в растворе. Рассмотрим это явление подробнее. [4]
Концентрация катализатора, изменяющего кинетические свойства системы, чаще всего ничтожна. Если катализатор с одним и тем же веществом может образовать как однотипно, так и различно построенные активные комплексы, то могут образоваться и различные конечные продукты. [5]
Вообще стабильность любого радикала определяется термодинамическими и кинетическими свойствами системы. Мерилом термодинамической стабильности радикала относительно реакции рекомбинации является разность свободных энергий AZ радикала и его димера. Эту разность нельзя отождествлять с разностью энергий стабилизации, с энергией сопряжения радикала, поскольку играют роль и энтропийные эффекты, связанные с различными значениями чисел степеней свободы, различными статсуммами радикала и димера. Кинетическая стабильность характеризуется тем активационным барьером, который нужно преодолеть при рекомбинации радикалов. Поэтому равновесие радикал-димер устанавливается с конечной скоростью, определяемой высотой барьера. Таким образом, можно говорить лишь об определенной стабильности радикала, стабильности относительно какого-либо процесса. Так, в равновесии радикал - димер Z 0, однако относительно другой системы, например радикал - растворитель, AZ 0 и тогда стабильность радикала определяется чисто кинетическими характеристиками такой системы. Например, трифенилметил стабилен при обычных условиях относительно диспропорционирова-ния и взаимного алкилирования, однако это чисто кинетическая стабильность, поскольку в присутствии катализаторов, под действием света, а также при повышенных температурах эти реакции идут необратимо с заметными скоростями. Стабильность радикала - понятие относительное и определяется совокупностью термодинамических и кинетических свойств рассматриваемой системы. [6]
Далее, Ро О т / й2 - диффузионный критерий Фурье, характеризующий внутренние кинетические свойства системы. [7]
В этой работе тепловые теории задержек зажигания сравниваются в условиях экзотермически реагирующей среды, поэтому тепловые и кинетические свойства системы являются определяющими. Решения ищутся в виде функций положения и времени, если среда стационарна, и в виде функций положения вдоль и поперек линий тока, если среда находится в ламинарном движении. В идеальном случае вид решения является явной функцией различных параметров, которая достаточно проста и определенна. Из-за сложного вида дифференциальных уравнений для теплообмена и присутствия в них нелинейных членов, представляющих скорость химической реакции, решение такого строгого вида получить не удается. [8]
Как видно из таблицы, наиболее существенным фактором, влияющим на выбор типа экстрактора, являются кинетические свойства системы и производительность. [9]
Настоящая работа предпринята с целью установить факт образования промежуточных валентностей при анодном окислении галлия и выяснить некоторые кинетические свойства системы галлий - ионы галлия. [10]
Химические реакции, в которые входит дополнительная компонента, не участвующая стехиометрически в суммарном процессе, но изменяющая кинетические свойства системы, называются каталитическими. [11]
Поскольку концентрация активного комплекса составляет лишь малую долю от концентрации исходных веществ, даже ничтожное количество катализатора часто меняет кинетические свойства системы. Например, для заметного изменения скорости окисления сернистокислого натрия в водном растворе достаточно 10 - 13 г-экв катализатора ( сернокислой меди) на 1 л раствора. [12]
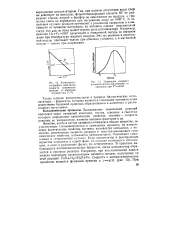 |
Зависимость логарифма константы скорости химической реакции от обратной температуры ( 1 / Т. [13] |
Явление, когда в состав активного комплекса входит вещество, не участвующее стехиометрически в суммарном процессе, но изменяющее кинетические свойства системы, называется катализом, а вещество, изменяющее скорость реакции и восстанавливающее свои химические свойства, называется катализатором. Различают гомогенный и гетерогенный катализ. Если катализатор и реагирующие вещества находятся в одной фазе, то катализ называется гомогенным, а если в различных фазах, то гетерогенным. В практике наблюдаются автокаталитические процессы, когда катализатор образуется в процессе реакции. Например, при восстановлении закиси железа водородом катализатором является железо, полученное по этой реакции: FeO - - H2 - - H2O - T-Fe. [14]
Поскольку концентрация активного комплекса составляет лишь малую долю от концентрации исходных веществ, даже ничтожное количество катализатора часто меняет кинетические свойства системы. Например, для заметного изменения скорости окисления сернистокислого натрия в водном растворе доста точно 10 - 13г - экв катализатора ( сернокислой меди) на 1 л раствора. [15]
Страницы: 1 2