Кислотное свойство - фенол
Cтраница 2
Кислотные свойства фенолов ослабляются при введении в кольцо заместителей I рода и усиливаются при введении заместителей II рода. [16]
Кислотные свойства фенолов ослабляются при введении в бензель ное кольцо электронодонорных заместителей и усиливаются при вве дении электроноакцепторных заместителей. Электронодонорные замес тители затрудняют делокализацию отрицательного заряда, тогда ка1 электроноакцепторные, наоборот, способствуют делокализации заря да и, следовательно, повышают кислотность. [17]
Однако кислотные свойства фенолов настолько слабы, что фенолы даже не изменяют цвета лакмусовой бумажки. [18]
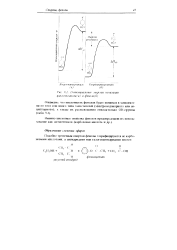 |
Потенциальные энергии ионизации циклогексанола ( а и фенола ( 6. [19] |
Именно кислотные свойства фенолов предопределили их. [20]
Однако кислотные свойства фенолов настолько слабы, что фенолы даже не изменяют цвета лакмусовой бумажки. [21]
Чем обусловлены кислотные свойства фенола. Какое соединение образуется при пропускании двуокиси углерода в водный раствор фенолята натрия. [22]
Вместе с тем кислотные свойства фенолов, в отличие от полиолов алифатического ряда, уменьшаются по мере увеличения числа гидроксильных групп, так как электронодоно-рные группы ОН ( М - эффект, превышающий - 1-эффект. О - Н и дестабилизируют полифенолят-анион. [23]
Благодаря присутствию галоидов кислотные свойства фенолов усиливаются, и, например, трнбромфенол является уже кислотой, вытесняющей угольную кислоту из углекислых солей. [24]
Благодаря присутствию галоидов кислотные свойства фенолов усиливаются, и, например, трибромфенол является уже кислотой, вытесняющей угольную кислоту из углекислых солей. [25]
Вместе с тем кислотные свойства фенолов, в отличие от тюлиолов алифатического ряда, уменьшаются по мере увеличения числа гидроксильных групп, так как электронодоно-рные группы ОН ( М - эффект, превышающий - 1-эффект. О - Н и дестабилизируют полифенолят-анион. [26]
При этом повышаются кислотные свойства фенолов и ароматических карбоно-вых кислот и уменьшается основность аминов. [27]
Такое же объяснение следует дать кислотным свойствам фенола. [28]
Определения констант диссоциации показывают, что кислотные свойства фенола выражены в 3300 раз слабее, чем у угольной кислоты. [29]
От присутствия нитрогруппы в фенолах усиливаются кислотные свойства фенола. Этим иногда пользуются для количественных определений. [30]
Страницы: 1 2 3 4