Кислотное свойство - карбоксильная группа
Cтраница 1
Кислотные свойства карбоксильной группы обусловлены отщеплением протона при электролитической диссоциации кислот. [1]
 |
Свойства монокарбоновык кислот. [2] |
Если радикал R содержит электроотрицательные группы, напр, атомы галогена ( у галогенкарбоновых к-т) или карбоксильную группу ( у дикарбоповых к-т), то отрыв протона облегчается и кислотные свойства карбоксильной группы усиливаются. [3]
 |
Свойства монокарбонов ых кислот. [4] |
Если радикал R содержит электроотрицательные группы, напр, атомы галогена ( у галогенкарбоновых к-т) или карбоксильную группу ( у дикарбоновых к-т), то отрыв протона облегчается и кислотные свойства карбоксильной группы усиливаются. [5]
На рис. 2 ( кривые 1 - 13) приведены кривые титрования эквимо-лярных смесей НС1 с различными аминокислотами раствором NaOH, имеющие два резких излома. Так как кислотные свойства карбоксильных групп амфолитов выражены довольно сильно, сначала наблюдается резкое понижение проводимости, что связано с нейтрализацией имеющихся в растворе ионов водорода и переходом катионов в биполярные ионы. После излома кондукто-метрической кривой протекает реакция вытеснения аминогрупп, что сопровождается повышением проводимости, так как при этом цвиттерионы переходят в анионы. [6]
Оксикислоты и дикарбоновые кислоты обладают повышенной растворимостью в воде. Последнее обстоятельство облегчает отрыв гидроксильного водорода, чем и обусловлены кислотные свойства карбоксильной группы. Ионизованная карбоксильная группа симметрична и ее кислородные атомы совершенно тождественны [ длина связи С - О составляет 0 127 нм ( 1 27 А. [7]
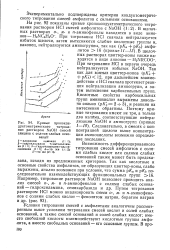 |
Кривые хронокондуктометрического титрования раствором NaOH смесей глицина с солями слабых оснований. [8] |
При титровании НС1 в первую очередь нейтрализуется избыток NaOH. Так как для взятых цвиттер-ионов ( рК а рК ь) 12, при-дальнейшем взаимодействии с НС1 сначала протекает реакция нейтрализации аминогрупп, а затем вытеснения карбоксильных групп. Кислотные свойства карбоксильных групп аминокислот выражены довольно сильно ( рК а 2 - т - 3), и реакции их вытеснения обратимы. Следовательно, в смесях с концентрацией щелочи выше концентрации аминокислоты возможно определение последних. [9]
Таким образом, если цвиттерионы характеризуются ( р / Са Р ь) 12 или меньше, при титровании сильными кислотами их смесей с щелочью сначала протекает реакция нейтрализации аминогрупп в анионах, а затем вытеснения карбоксильных групп в цвиттерионах. Однако только первая реакция протекает количественно. Кислотные свойства карбоксильных групп типичных цвиттерионов выражены довольно сильно ( р / ( а 2н - 3) и реакция вытеснения обратима. Поэтому кондуктометрические кривые имеют только один излом, соответствующий окончанию реакции нейтрализации, после чего наблюдается нелинейное повышение электропроводности раствора, что свидетельствует об обратимости реакции вытеснения карбоксильных групп. [10]
Из приведенного уравнения видно, что при гидролизе число концевых карбоксильных групп увеличивается, в то время как при термолизе оно остается почти неизменным. Это позволяет следить за ходом гидролиза посредством титрования растворов желатина щелочью. Но в водной среде кислотные свойства карбоксильных групп ослабляются присутствием основных аминогрупп, поэтому в водной среде титрование щелочью не идет до конца. Лучшие результаты дает титрование в спиртовой среде, так как в присутствии спирта кислотные свойства карбоксильных групп преобладают над основными свойствами аминогрупп. [11]
С ] 0, они практически нерастворимы в воде и являются кристаллич. Оксикислоты и дикарбоновые кислоты обладают повышенной растворимостью в воде. Последнее обстоятельство облегчает отрыв гидроксильного водорода, чем и обусловлены кислотные свойства карбоксильной группы. [12]
Сульфопропионовая кислота и ее производные. Кислые соли являются слабыми кислотами [380], вероятно, не более сильными, чем пропионовая кислота. Возможно, что производное нейтральной функции, например сульфамидная группа, повысило бы кислотные свойства карбоксильной группы, но сульфогруппа повышения не вызывает. [13]
Сульфопропионовая кислота и ее производные. Кислые соли являются слабыми кислотами [380], вероятно, не более сильными, чем пропионовая кислота. Возможно, что производное нейтральной функции, например сульфамидная группа, повысило бы кислотные свойства карбоксильной группы, но сульфогруппа повышения не вызывает. [14]
Из приведенного уравнения видно, что при гидролизе число концевых карбоксильных групп увеличивается, в то время как при термолизе оно остается почти неизменным. Это позволяет следить за ходом гидролиза посредством титрования растворов желатина щелочью. Но в водной среде кислотные свойства карбоксильных групп ослабляются присутствием основных аминогрупп, поэтому в водной среде титрование щелочью не идет до конца. Лучшие результаты дает титрование в спиртовой среде, так как в присутствии спирта кислотные свойства карбоксильных групп преобладают над основными свойствами аминогрупп. [15]
Страницы: 1 2