Электролитическое свойство
Cтраница 1
Электролитические свойства воды, определяются присутствующими в воде растворенными примесями, а также показателем концентрации водородных ионов рН, Чистая вода является слабым электролитом. [1]
Другие электролитические свойства, например гидролиз, образование комплексных соединений для элементов, начиная с Cm, в седьмом периоде, имеют также отдаленное сходство в свойствах при сравнении с лантанидами. Действительно известно, что характерной чертой протактиния является слабая основность, большая склонность к гидролизу и очень малая растворимость его соединений в растворах, в которых не образуются комплексные соединения. [2]
Электролитические свойства расплавленных силикатов, в частности стекол при повышенных температурах, как униполярных проводников, вызывают ряд явлений, характеризующихся возникновением гальванических потенциалов на фазовых границах стекла с другой средой, например с расплавленными солями или водными растворами. I, § 107 и ниже), потенциалы на границе с расплавленными солями должны быть рассмотрены здесь, ввиду их важного практического значения для стеклянных электродов. Следует упомянуть, что на стеклянных электродах возникает асимметричный потенциал, который, согласно Брауеру1 и Кратцу2, объясняется несоблюдением необходимых правил при термической обработке стекла и специфическим влиянием, атмосферы газов при отжиге. [3]
Электролитические свойства соединений пятивалентного мышьяка и сурьмы еще не изучены, однако химические свойства пентагалогенидов сурьмы и тристрифторметильных производных пятивалентной сурьмы очень сходны между собой. [4]
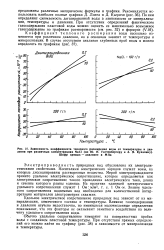 |
Зависимость коэффициента теплового расширения воды от температуры и давления при различных концентрациях NaCI ( no Ю. П. Гаттенбергеру и А. Я. Кулапину. Шифр кривых - давление в МПа. [5] |
Электропроводность природных вод обусловлена их электролитическими свойствами. Носителями электрических зарядов служат ионы, на которые диссоциированы растворенные вещества. Мерой электропроводности принято удельное электрическое сопротивление, которое определяется как электрическое сопротивление такого проводника электрического тока, длина и сечение которого равны единице. Знание удельного сопротивления подземных вод необходимо для количественной интерпретации материалов электрометрии скважин. [6]
 |
Допустимые концентрации кальция в зависимости от аналитически определяемой концентрации сульфатов в воде. [7] |
Как показали исследования последних лет, электролитические свойства солей в воде высоких параметров заметно изменяются. Вода высокой температуры ( более 300 С) из-за снижения диэлектрической проницаемости становится не столь сильно ионизирующим растворителем, в связи с чем степень диссоциации солей в воде высокой температуры уменьшается. Сплошная кривая рассчитана [7.1] с учетом изменения электролитических свойств солей в воде высоких параметров. Пунктирная кривая получена для условий полной диссоциации солей. Относительное расположение кривых на рис. 7.1 показывает, что вычисления допустимых концентраций кальция без учета частичной ассоциации ионов дают заметно заниженные результаты. В области небольших солесо-держаний концентрация сульфатов в силь-ной степени сказывается на допустимой концентрации кальция в котловой воде. [8]
Начиная с середины 60 - х годов электролитические свойства уже известных и вновь создаваемых материалов стали предметом интенсивных исследований. [9]
С изменением температуры и давления меняются также электролитические свойства воды. [10]
Устойчивость, текучесть и водосодержание шликеров определяются электролитическими свойствами суспензии и состоянием связи минеральных частиц с водой. [11]
 |
Стеклянный электрод. [12] |
Иногда внутренняя и внешняя поверхности стеклянного шарика бывают различны по своим электролитическим свойствам, поэтому возникает потенциал асимметрии, который искажает результат измерения. [13]
Большой практический интерес представляет синтез соединений, которые сохраняли бы структурную разупорядоченность и связанные с ней электролитические свойства при комнатной температуре. Иодид серебра оказался подходящим базисным соединением для этой цели; на его основе синтезировано несколько десятков твердых электролитов, удовлетворяющих поставленному требованию. Это достигается добавлением к иоди-ду серебра каких-либо ионов, стабилизирующих кубическую структуру и препятствующих се превращению при низких температурах в гексагональную, плотноупакованную по анионам. [14]
Не подлежит никакому сомнению, что также и между очень тонко и грубо кристаллическими массами металла существуют различия в электролитических свойствах. При точке превращения или точке плавления обе фазы не могут давать тока, так как тогда они находятся между собой в равновесии. Образующая при этой температуре теплота превращения или плавления, следовательно, не может быть превращена в электрическую энергию. [15]
Страницы: 1 2