Парциальное мольное свойство
Cтраница 2
Это название сохраняется для коэффициентов разложения в ряд Тейлора парциального мольного свойства растворенного вещества по его мольной доле. Коэффициенты рядов (7.24) - (7.26) можно, однако, легко рассчитать, используя параметры взаимодействия, с помощью уравнения Гиббса - Дюгема. [16]
Даже для расчета мольных свойств, не говоря уже о парциальных мольных свойствах, требуются не столько непосредственные экспериментальные данные р - у - т - N, сколько различные производные ( первые, если не вычислять Ср и Cv) от этих данных. [17]
В отличие от (10.26) одинаковый набор аргументов функций Иг и Hi является в данном случае естественным, поскольку любые парциальные мольные свойства зависят только от переменных Т, Р, п ( точнее, от Т, Р, х) ( ср. [18]
В этой записи подФ / подразумевается либо мольное свойство 1-го компонента, если он образует отдельную фазу, либо парциальное мольное свойство, если он находится в растворе или газовой смеси. [19]
При анализе сложных систем в процессе при постоянных температуре и давлении ( Т, р const) полезным является понятие парциального мольного свойства. [20]
Поэтому для компонента раствора справедливы те же уравнения, что и для чистою вещества, но только вместо мольных свойств в них фигурируют соответствующие парциальные мольные свойства. [21]
Поэтому для компонента раствора справедливы те же уравнения, что и для чистого вещества, но только вместо мольных свойств в них фигурируют соответствующие парциальные мольные свойства. [22]
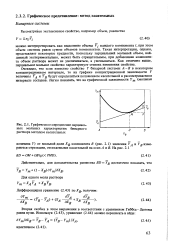 |
Графическое определение парциальных мольных характеристик бинарного раствора методом касательных. [23] |
Такая интерпретация, однако, представляет некоторые трудности, поскольку парциальный мольный объем, найденный экспериментально, может быть отрицательным, при добавлении компонента объем раствора может не увеличиваться, а уменьшаться. Как отмечено выше, парциальное мольное свойство характеризует степень изменения свойства. [24]
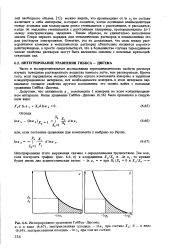 |
Интегрирование уравнения Гиббса-Дюгема. [25] |
Часто в экспериментальном исследовании термодинамических свойств раствора изучать поведение растворенного вещества намного легче, чем растворителя. Кроме того, если парциальное мольное свойство одного компонента измерено в заданном концентрационном интервале, нет необходимости измерять в этом интервале парциальное мольное свойство другого компонента: его можно найти с помощью уравнения Гиббса-Дюгема. [26]
Уравнение (IV.8) показывает, что экстенсивное свойство раствора определяется количествами и парциальными мольными величинами отдельных компонентов. Если состав раствора изменяется, то изменяются и парциальные мольные свойства. [27]
Объемные термодинамические свойства жид -, костей наиболее непосредственно связаны с упаковкой молекул и изменениями этой упаковки при изменении параметров состояния. Поскольку любые изменения структуры растворителя должны давать вклад в парциальные мольные свойства растворенного вещества в разбавленном растворе, то изучение объемных характеристик разбавленных водных растворов неэлектролитов - важный способ исследования их строения. В этом разделе рассматриваются данные о предельных значениях парциальных мольных и парциальных избыточных объемов полярных неэлектролитов в воде, а также о зависимости этих величин от температуры и давления. [28]
Уравнение ( 17) связывает с мольными свойствами и составом раствора парциальные мольные свойства всех компонентов, кроме одного, мольная доля которого была исключена. [29]
Часто в экспериментальном исследовании термодинамических свойств раствора изучать поведение растворенного вещества намного легче, чем растворителя. Кроме того, если парциальное мольное свойство одного компонента измерено в заданном концентрационном интервале, нет необходимости измерять в этом интервале парциальное мольное свойство другого компонента: его можно найти с помощью уравнения Гиббса-Дюгема. [30]
Страницы: 1 2 3