Типичное свойство - металл
Cтраница 1
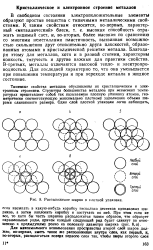 |
Расположение шаров в ллотной упаковке. [1] |
Типичные свойства металлов обусловлены нх кристаллическим и электронным строением. Структура большинства металлов при невысоких температурах представляет собой так называемую плотную упаковку атомов, геометрически соответствующую максимально плотному заполнению объема шарами одинакового размера. [2]
Типичными свойствами металлов являются блестящая поверхность, ковкость, высокая электро - и теплопроводность. Прохождение электрического тока осуществляется за счет электронов и не сопровождается химическими изменениями. Металлы практически нерастворимы в воде. [3]
Если типичные свойства металлов определили их применение в качестве конструкционных материалов, то для механической обработки металлов потребовались материалы - инструментальные и абразивные - с иными свойствами. Инструментальные и абразивные материалы должны отличаться от конструкционных ( металлических) материалов большей механической прочностью, твердостью, термической и химической стойкостью. Оказалось, что такие свойства могут иметь вещества, кристаллические решетки которых в отличие от металлических относятся к атомному типу. Такой тип кристаллических решеток встречается у элементарных веществ и простых соединений, образованных химическими элементами промежуточного характера, к которым относятся бор, углерод, кремний, германий, сурьма. [4]
К типичным свойствам металлов относятся: поверхностный блеск, ковкость, высокая электропроводность и теплопроводность. Носителями тока являются электроны, причем электрический ток не сопровождается химическими изменениями. Металлы практически нерастворимы в воде. [5]
Расплавленные металлы обладают всеми типичными свойствами металлов. Это значит, что металлическая структура свойственна не только кристаллам. Она не разрушается и в аморфных жидкостях. С этим, между прочим, связана растворимость металлов в расплавленных металлах, так как в этом случае, и только в этом случае, удовлетворяется правило химического подобия, которому подчинено растворение. [6]
Представление о подвижных электронах хорошо объясняет наиболее типичное свойство металлов - их высокую электропроводность. [7]
Обратите внимание на другое важное свойство гидридов внедрения: при их образовании сохраняются такие типичные свойства металлов, как металлический блеск, электропроводность. Правда, они выражены слабее, чем у исходных металлов. Например, у них значительно ниже пластичность - насыщенные водородом металлы делаются хрупкими, часто исходные металлы нелегко измельчить в порошок, а с гидридами тех же металлов это сделать гораздо легче. Но все-таки гидриды внедрения несравненно больше похожи на исходные металлы, чем, скажем, гидриды щелочных и щелочноземельных металлов. [8]
Несмотря на то что, как указывалось выше, Li в большинстве случаев проявляет типичные свойства металлов I группы, существуют некоторые отличия, которые сближают его с магнием. Аномальные свойства Li являются главным образом следствием небольшого размера его атома и иона; поляризующая способность Li -, наивысшая среди ионов щелочных металлов, приводит к необычайно высокой сольватации и образованию ковалентной связи. [9]
Несмотря на то что, как указывалось выше, Li в большинстве случаев проявляет типичные свойства металлов I группы, существуют некоторые отличия, которые сближают его с магнием. Аномальные свойства Li являются главным образом следствием небольшого размера его атома и иона; поляризующая способность Li, наивысшая среди ионов щелочных металлов, приводит к необычайно высокой сольватации и образованию ковалентной связи. [10]
Кальций, стронций и барий известны под общим названием щелочноземельных металлов. Из металлов II группы они наиболее активны, проявляют типичные свойства металлов, хотя и несколько слабее выраженные, чем у щелочных металлов. [11]
Кальций, стронций и барии известны под общим названием щелочноземельных металлов. Из металлов II группы они наиболее активны, проявляют типичные свойства металлов, хотя и несколько слабее выраженные, чем у щелочных металлов. В соединениях они положительно двухвалентны. Ионов с другой положительной валентностью или отрицательно валентных ионов не образуют. На воздухе легко окисляются, давая оксиды основного характера состава ЭО. Химическая активность оснований последовательно возрастает от кальция к барию. Наиболее энергично из них разлагает воду барий. [12]
Кальций, стронций и барий известны под общим названием щелочноземельных металлов. Из металлов II группы они наиболее активны, проявляют типичные свойства металлов, хотя и несколько слабее выраженные, чем у щелочных металлов. В соединениях они положительно двухвалентны. Ионов с другой положительной валентностью или отрицательно валентных ионов они не образуют. На воздухе легко окисляются, образуя окислы основного характера состава RO. Химическая активность оснований последовательно возрастает от кальция к барию. Наиболее энергично из них разлагает воду барий. [13]
Металлы имеют кристаллические решетки, построенные из положительно заряженных ионов, в промежутках между ними находятся валентные электроны - металлические решетки. Валентные электроны, переходя от одного иона к другому, осуществляют между ними достаточно прочную связь. Эти подвижные электроны определяют типичные свойства металлов - высокую теплопроводность и электропроводность, хорошую пластичность даже в холодном состоянии. [14]
От электролитов электронные полупроводники отличаются иной физической природой носителей тлка. От металлов они отличаются не только меньшей величиной электропроводности ( меньшей чем 104 ом - 1-см - 1), но и иной ее зависимостью от температуры: в то время как электропроводность металлов с понижением температуры растет, а с приближением к абсолютному нулю достигает весьма больших значений или даже переходит в сверхпроводимость, полупроводники с понижением температуры обычно уменьшают свою проводимость, а вблизи абсолютного нуля становятся изоляторами. Большая или бесконечно большая величина проводимости вблизи абсолютного нуля - типичное свойство металла, указывающее, что тепловое движение не является в этом случае причиной, вызывающей проводимость и только создает препятствие движению электронов, тогда как электроны проводимости полупроводника появляются в результате теплового движения. [15]
Страницы: 1 2