Восстановительное свойство - атом
Cтраница 1
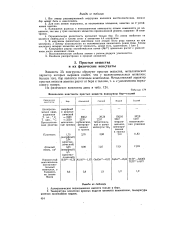 |
Физические константы простых веществ подгруппы бор-таллий. [1] |
Восстановительные свойства атомов с ростом радиуса усиливаются. [2]
В подгруппах аналогов восстановительные свойства атомов растут параллельно с ростом радиуса и уменьшением ионизационного потенциала. В подгруппах 1А, 2А, 3В, ЗА и всех / - элементов восстановительная активность возрастает сверху вниз, у d - элементов, кроме подгруппы 3В, - снизу вверх. [3]
В периодах, если двигаться по таблице слева направо, восстановительные свойства атомов падают. Наиболее сильный восстановитель в каждом периоде - это щелочной металл, наиболее слабый - галоген. [4]
При этом легко убедиться в том, что степень окисления атома азота как в молекуле аммиака, так и в ионе аммония одна и та же, именно равная - III, поэтому восстановительные свойства атома азота в обеих частицах примерно одни и те же. [5]
В тесной связи с ионизационными потенциалами находятся восстановительные свойства атомов. [6]
Атомарный водород, как правило, проявляет восстановительные свойства. Его восстановительное действие определяется реакционной способностью растворенного вещества, а также зависит от рН среды. С увеличением рН восстановительные свойства атомов Н становятся более резко выраженными. В кислых растворах атомы Н могут проявлять окислительные свойства. [7]
Атомарный водород, как правило, проявляет восстановительные свойства. Его восстановительное действие определяется реакционной способностью растворенного вещества и зависит от рН среды. С увеличением рН восстановительные свойства атомов Н становятся более резко выраженными. В кислых растворах атомы Н могут проявлять окислительные свойства. [8]
У германия появляются некоторые черты металличности. От углерода к свинцу ослабляются окислительные и усиливаются восстановительные свойства атомов. У соединений четырехвалентных элементов по тому же ряду усиливаются окислительные свойства, а у соединений двухвалентных элементов ослабляются восстановительные свойства. [9]
Первые два элемента - типичные неметаллы. У германия появляются некоторые черты металличности. От углерода к свинцу ослабляются окислительные и усиливаются восстановительные свойства атомов. У соединений четырехковалентных элементов по тому же ряду усиливаются окислительные свойства, а у соединений элементов ( II) ослабляются восстановительные свойства. [10]
Энергия ионизации является очень важной характеристикой атомов. Энергия ионизации определяет также восстановительные свойства атомов, поскольку чем меньше энергия ионизации, тем легче атом отдает электрон. [11]
Энергия ионизации является очень важной характеристикой атомов. Энергия ионизации определяет также восстановительные свойства атомов, поскольку чем меньше энергия ионизации, тем легче атом отдает электрон. [12]
Энергия ионизации является очень важной характеристикой атомов. Как мы увидим в дальнейшем, от нее в значительной степени зависят характер и прочность химической связи. От энергии ионизации зависят также восстановительные свойства атомов, поскольку чем меньше энергия ионизации -, тем легче атом отдает электрон. [13]
Энергия ионизации является очень важной характеристикой атомов. Как мы увидим в дальнейшем, от нее в значительной степени зависят характер и прочность химической связи. От энергии ионизации зависят также восстановительные свойства атомов, поскольку чем меньше энергия ионизации, тем легче атом отдает электрон. [14]
Энергия ионизации является очень важной характеристикой атомов. Как мы у видим в дальнейшем, от нее в значительной степени зависят характер и прочность химической связи. От энергии ионизации зависят также восстановительные свойства атомов, поскольку чем меньше ионизационный потенциал, тем легче атом отдает электрон. [15]
Страницы: 1